大動脈弁狭窄症とは、心臓の弁のひとつがちゃんと開かず、心臓から全身に血液が送り出しにくくなってしまう病気です。
進行すると、狭心痛や心不全などを起こします。また、安静時でも息切れの症状が現れ、最終的には突然死にいたることもあります。無症状の時期が長く続き、症状が現われるようになってからは、一般に予後が不良です。
ここでは、大動脈弁狭窄症がどうして起こるのか、どういう症状が現われるのか、どう治療するのか、などについて説明します。
目次
大動脈弁狭窄症とは
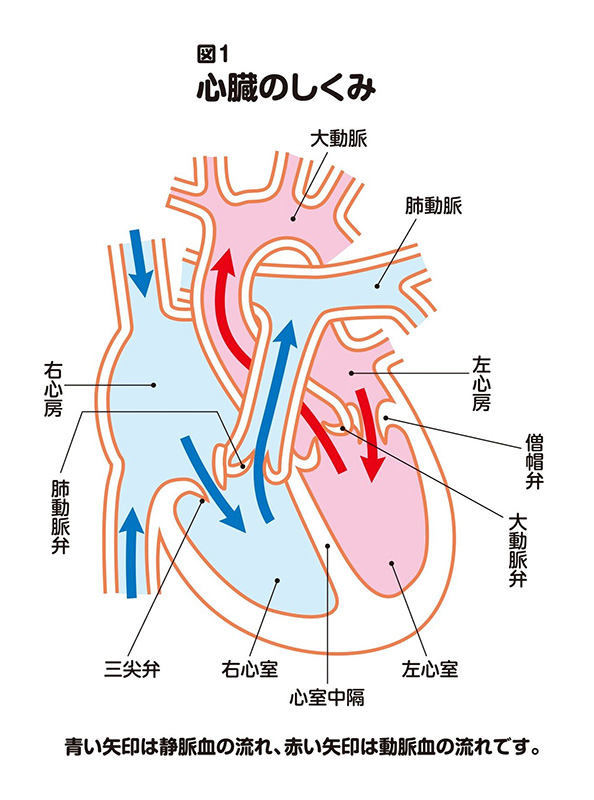
大動脈弁狭窄症とは、心臓の弁のひとつである大動脈弁がきちんと開かなくなる病気です。 心臓には、三尖[さんせん]弁、肺動脈弁、僧帽[そうぼう]弁、大動脈弁の4つの弁があります。そのひとつの大動脈弁は、左心室(左室)と大動脈の間にあって、肺で酸素が豊富に取り込まれた血液(動脈血)を、左室から大動脈経由で全身に送り出す際の関門の役割を果たしています(図1)。
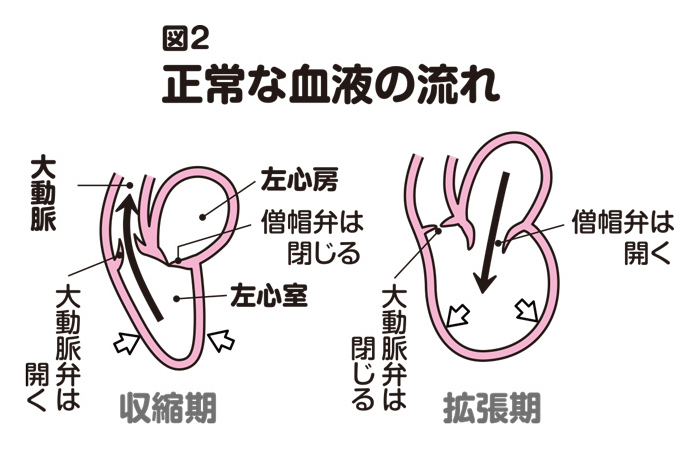
大動脈弁は心臓の収縮期に開いて、左室から大動脈に血液を送り出し、拡張期には閉じて、左心房(左房)から僧帽弁を通して送り込まれる血液が、左室に満たされるのを助けます(図2)。
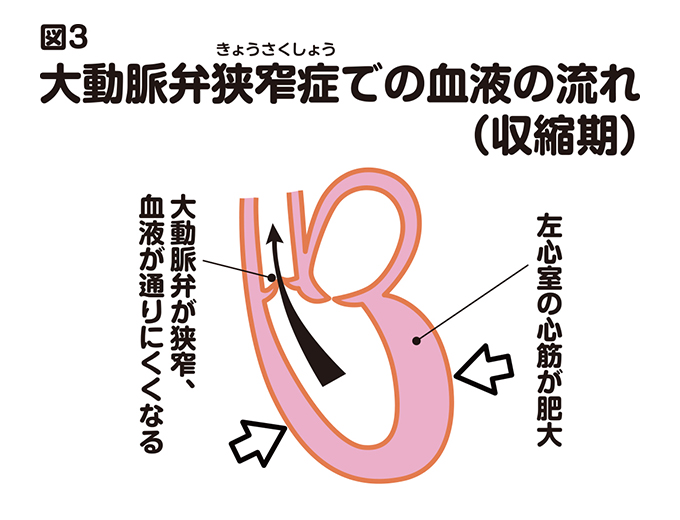
ところが、なんらかの原因で大動脈弁が損なわれ、動きが悪くなって、収縮期にきちんと開かなくなると、弁口が狭まって(狭窄して)、左室から大動脈に血液が送り出しにくくなります(図3)。その結果、左室に大きな負担がかかるようになり、進行すると心不全(心臓のポンプ機能の低下)を引き起こします。これが大動脈弁狭窄症です。英語ではaortic stenosisと言います(略してASと呼ぶことがあります)。
大動脈弁はどのように狭窄するのか
大動脈弁が狭窄するのは、弁が硬くなったり、くっついたりするからです。
大動脈弁の弁尖(扉の役割を果たしている半月形の膜)や交連部(弁尖と弁尖の境目の部分)に、そうした異常が生じます。
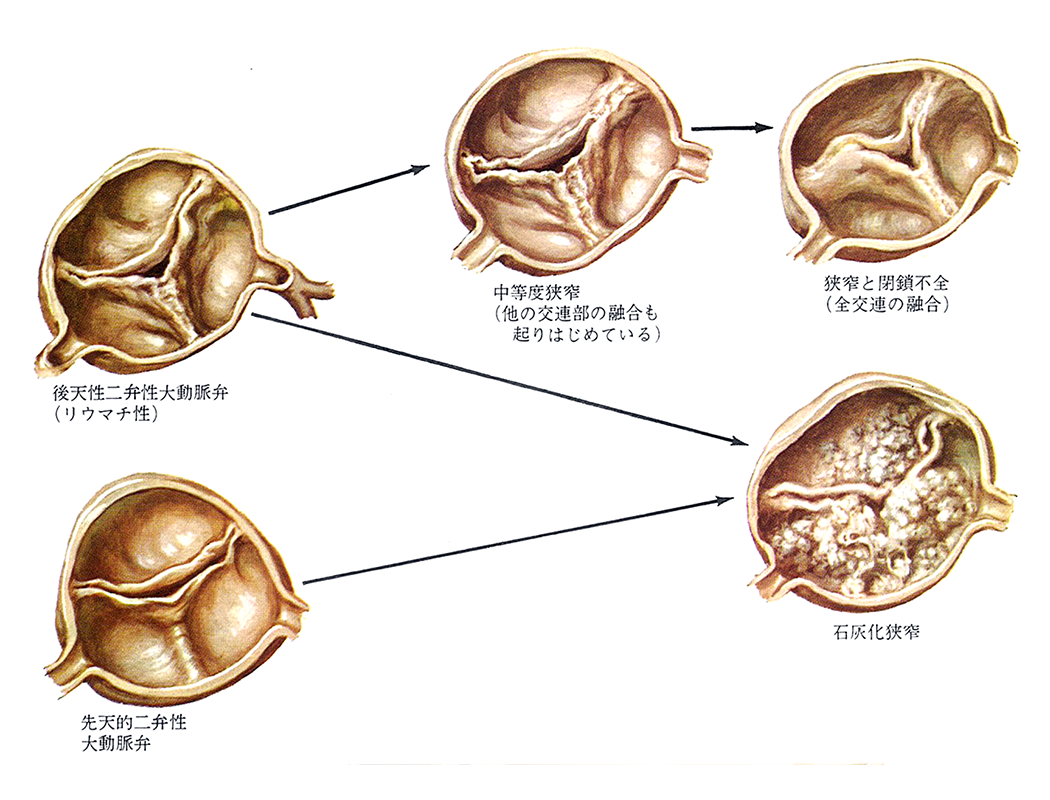
弁尖は、石灰化(カルシウムなどが沈着し弾力性や柔軟性を失った状態)したり肥厚したりすると、硬くなります。交連部で、隣り合った弁尖がくっついてしまう(癒合してしまう)こともあります。そうなると、弁口面積が狭くなってしまうのです(図4)。
大動脈弁狭窄症を引き起こす原因
大動脈弁狭窄症を引き起こす原因には、先天的な(生まれつきの)もの、動脈硬化によるもの、リウマチ熱の後遺症などがあります。
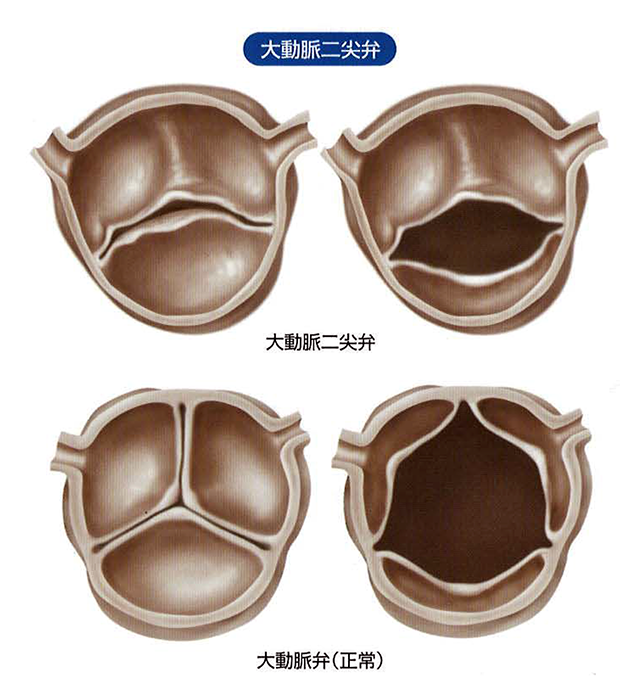
先天的なものの代表は、二尖[にせん]弁です。大動脈弁の弁尖は本来3枚あるのですが、生まれつきこれが2枚しかない人がいます(図5)。弁尖が2枚しかないと、狭窄しやすくなります。比較的若い年齢層で見られます。
高血圧や糖尿病、高脂血症などを抱えていると動脈硬化が進みがちですが、大動脈弁でも動脈硬化は起こり、そうなると弁尖は石灰化します。多くの高齢者に、加齢によって硬化・石灰化した大動脈弁狭窄症が見られます。
リウマチ熱というのは、溶血性連鎖球菌(溶連菌)による咽頭炎が引き起こす全身性の自己免疫疾患です。発熱や関節炎だけでなく、心筋(心臓の筋肉)の組織も侵し、弁にも炎症を起こします。ほとんどは小児期にかかるのですが、成人してから、その後遺症として大動脈弁狭窄症が出現することがあります。交連部の癒合が特徴です。
近年は、抗菌薬の普及や衛生環境の向上もあって、リウマチ性の動脈弁狭窄症は減少しています。一方で、高齢化に伴う石灰化性の大動脈弁狭窄症が増えてきています。
大動脈弁狭窄症の症状
大動脈弁狭窄症になっても、しばらくはほとんど症状が出ません。
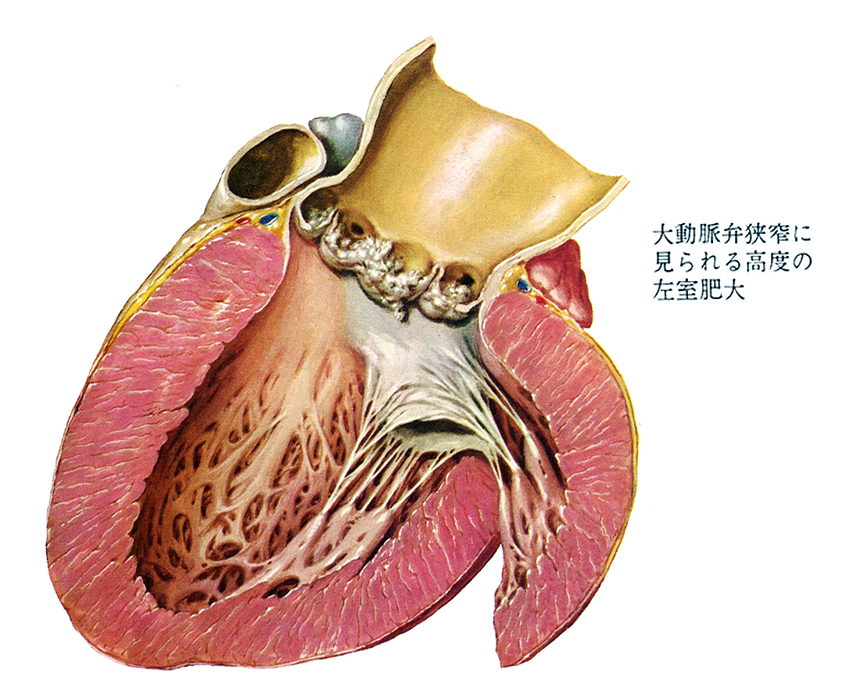
大動脈弁狭窄症を起こすと、血液が左室から大動脈に流れにくくなるため、左室に大きな負荷がかかり、左室の心筋が分厚くなります(これを「心筋の肥大」と言います)(図6)。しかし、ポンプ機能を維持しようとする代償機構が働くので、症状としては現われてこないのです。
それでも、やがては代償機構が働くのにも限界がきて、左室の壁が拡大し、収縮力が弱まって心臓の機能が低下するようになります。
大動脈弁狭窄症の主な症状は、息切れ、動悸、足のむくみ、身体がだるく疲れやすくなる、失神、狭心痛(胸の痛み)、呼吸困難です(これらがすべて現われるわけではありません)。
大動脈弁狭窄症の症状①失神
失神が起こるのは、血流が低下するからです。
大動脈弁狭窄症が進行すると、ポンプ機能が低下して、左室から大動脈に送り出される血液の量が減ります。そうなると、階段や坂道を上ったり、ちょっとした荷物を持ったりしたときでも、末梢血管が拡張して血圧が下がり、脳の血流も低下して、めまいや失神が引き起こされるのです。
大動脈弁狭窄症の症状②狭心痛(胸の痛み)
狭心痛が起こるのは、心筋に充分な血液が行かなくなるからです。
左室が肥大すると、心筋での酸素の需要が増えます。しかし、大動脈弁狭窄症で血流が低下していると、冠[かん]動脈(心臓の表面を走っている、心筋に酸素や栄養を送る血管)の血流も低下します。そのため、心筋への酸素の補給が間に合わなくなり、狭心痛が起こるのです(狭心痛が起こる状態を狭心症と言います)。
大動脈弁狭窄症の症状③呼吸困難
呼吸困難が起こるのは、左[さ]心不全を起こしているからです。
心不全は、心臓のポンプ機能が低下した状態です。主に左心系(左室・左房の総称)が原因となって引き起こされる心不全を、左心不全と言います。
左心不全を起こすと、血液が左心系に滞留するようになります。そうなると、血流の上流である肺にも影響が及んで、肺に血が溜まったり(肺うっ血)、水が溜まったり(肺水腫)します。その結果、肺での二酸化炭素と酸素の交換が効率よく行なわれなくなり、肺も膨らみにくくなって、呼吸困難が生じるのです。また、下肢などにむくみも出たり、運動中に疲労感や息切れを起こしたりします。
大動脈弁狭窄症は突然死を招くことも
大動脈弁狭窄症の特徴のひとつに、突然死があります。
大動脈弁狭窄症が進行し、失神、狭心痛、呼吸困難などの症状が出現するようになると、突然死の危険性が高まります。重篤な症状が出ている場合、症状を自覚してから2~3年で突然死するケースがよく見られます。
合併症について
大動脈弁狭窄症では、まれに感染性心内膜炎を合併することがあります。
感染性心内膜炎とは、血液が大動脈に送り出される際に通過障害により生じた血流のジェット(乱流)が、大動脈弁を傷つけ、その傷に血液中の細菌が感染し炎症を起こしたものです。弁が破壊されるだけでなく、細菌の塊が動脈を塞いだり、脳梗塞を引き起こしたりもします。
大動脈弁狭窄症の人が、歯科や耳鼻科の治療、内視鏡手術など、細菌が血液に混入する可能性のある処置をするときには、あらかじめ抗生物質を服用し、感染性心内膜炎が発症しないようにする必要があります。
大動脈弁狭窄症の重症度分類
大動脈弁狭窄症の重症度は、心エコー(超音波)検査や心カテーテル検査を行なって得たデータを基に評価します(表1)。
弁口面積、最高血流速度、収縮期平均圧較差の3つを測定します。
| 軽度 | 中等度 | 高度 | |
|---|---|---|---|
| 連続波ドプラ法による 最高血流速度(m/s) |
<3.0 | 3.0-4.0 | ≧4.0 |
| 簡易ベルヌイ式による 収縮期平均圧較差(mmHg) |
<25 | 25-40 | ≧40 |
| 弁口面積(cm2) | >1.5 | 1.0-1.5 | ≧1.0 |
(日本循環器学会 弁膜疾患の非薬物治療に関するガイドライン[2007年改訂版]より抜粋)
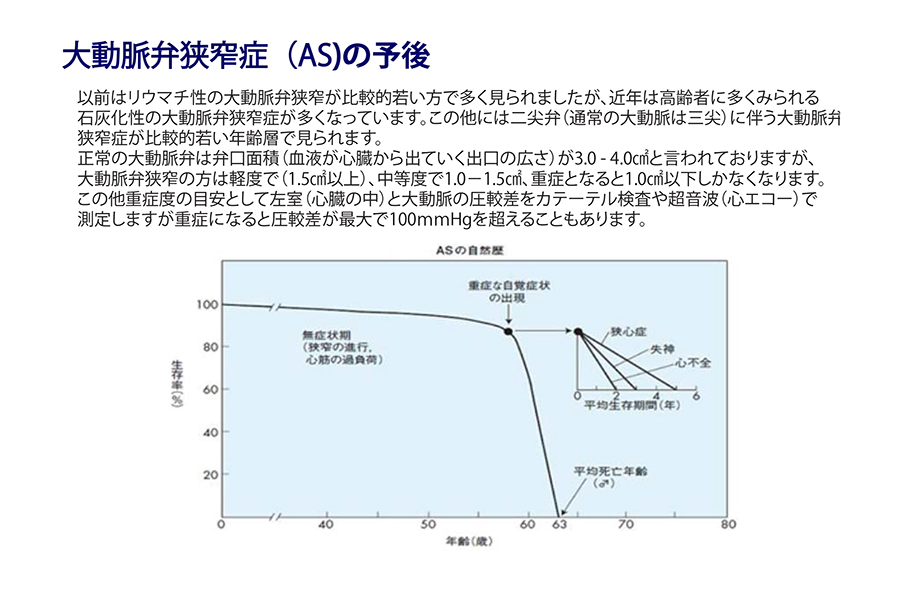
大動脈弁狭窄症は長年無症状で経過します。しかし弁の狭窄は進行することはあっても改善することはありません。
一旦、心不全などの重篤な症状が出た場合、突然死などで死亡されるまでの期間は短く、2-3年以内に多くの方がなくなるといわれております。
大動脈弁狭窄症は進行する病気なので、重症度の変化を把握するために定期的な検査を行う必要があります。
弁口面積
弁口面積とは、心臓の収縮期に大動脈弁が開いている面積(血液の出口の広さ)で、心エコー検査で測定します。正常な大動脈弁の弁口面積は3.0~4.0㎠と言われているのですが、大動脈弁狭窄症が軽度の人ではこれが1.5㎠以上、中等度では1.0~1.5㎠、高度(重症)となると1.0㎠以下にまで狭くなってしまいます。
最高血流速度
最高血流速度とは、収縮期に大動脈弁を流れる血液の最高速度で、心エコー検査のひとつであるドプラ法で測定します。軽度であれば1秒間に3.0mの速度、中等度であれば3.0~4.0mの速度、高度になると4.0mを超える高速になります。
収縮期平均圧較差
収縮期平均圧較差とは、収縮期における左室と大動脈との間の圧力の差で、大動脈と左室にカテーテル(細い管)を入れる心カテーテル検査や、連続ドプラ法で測定します。軽度であれば25mmHg以下、中等度であれば25~40mmHg、高度になると40mmHg以上で、ときには100mmHgを超える人もいます。
診断・検査
大動脈弁狭窄症の診断・検査には、聴診、心電図、胸部エックス線検査、心エコー(超音波)検査、心カテーテル検査などが用いられます。
聴診
聴診器を当てると、収縮期駆出性雑音という特有の心雑音が聞き取れます。血液が大動脈に送り出される(駆出される)収縮期に、通過障害により血流のジェット(乱流)が生じることが原因です。音は、だんだん大きくなったあと次第に小さくなります。狭窄が進めば進むほど音が大きくなります。
心電図
心臓から出る電気信号をグラフ化する検査で、左室の肥大の程度、左脚ブロック(拍動を命ずる電気信号が左室に伝わっていない状態)の有無などが分かります。
胸部エックス線検査
エックス線を当てて心臓の内部を探る検査です。大動脈弁狭窄症を起こしてからしばらくは、左室は、肥大はするものの代償機構が働いて拡大しませんが、代償機序が破綻すると、拡大するようになります。この検査では、その左室の拡大や上行大動脈の拡大などが観察できます。
心エコー検査
人間の耳には聞こえない超音波(エコー)を用いて心臓の内部を探る検査で、断層心エコー法、経食道エコー法、ドプラ法などがあります。重症度を測る指標の弁口面積は、この心エコー検査で求めます。
そして、左心室の機能を検査する上で最も良い方法です。
大動脈弁狭窄症の重症度が中等症以下であれば、定期的な心エコー検査と感染性心内膜炎の予防で十分です。しかし、狭窄は徐々に進行していくため注意してください。半年から1年ごとの定期的な心エコー検査で経過観察が必要となります。
断層心エコー法は、心臓の断層を連続撮影するものです。この検査で弁尖の石灰化や肥大、可動性の程度、左室の肥大の様子など、さまざまな情報を読み取ります。
経食道エコー検査は、断層心エコー法では不十分な情報しか得られないときに用いられる検査で、超音波プローベ(探触子)を食道に飲み込んで行ないます。断層心エコー法が胸壁を隔てた検査であるのに対し、こちらはより近い心臓の裏側から探る検査なので、断層心エコー法よりも詳しい情報が得られるのです。
ドプラ法は、心臓内の血流の速度と方向を測定する検査で、重症度を測る指標の最高血流速度は、この検査で求められます。また、連続波ドプラ法を用いると、収縮期平均圧較差をベルヌーイの式によって簡易的に求めることができます。
心臓カテーテル検査
大動脈経由で左心室まで挿入したカテーテルを、左室から大動脈に引き抜くことで左室と大動脈の圧力の差を計測する検査です。重症度を測る指標の収縮期平均圧較差は、この検査で求められますが、近年は、心エコー検査の進展であまり行なわれなくなりました。
しかし、大動脈弁狭窄症にもかかわらず症状が出ない人では、負荷試験が行なわれることがあります。試験中に狭心症、息切れ、失神が起こる人は、治療が必要と判断されます。
手術適応
大動脈弁狭窄症の手術適応は、症状が出ている患者さんです。
ただし、症状が出ていなくても、各種の検査で心臓の機能に低下が見られる方や透析治療を受けている方は病気の進行が速いので、早めに手術を検討します。
大動脈弁狭窄症の治療・手術方法
大動脈弁狭窄症の治療には、内科治療と外科治療があります。内科治療では薬物による治療を行ない、外科治療では手術を行ないます。
大動脈弁狭窄症の内科治療
大動脈弁狭窄症が軽度であれば、内科治療で全身状態を管理し、経過観察を行ないます。しかし、長期的に見て有効な内科治療がないのが現実です。弁の狭窄は薬では治りません。ただし、手術のできない患者さんの症状コントロールには、内科治療が必須です。
なお、心不全を起こしている大動脈弁狭窄症の患者さんには、原則として利尿薬は用いません。通常、心不全のコントロールには、血液の量を減らし血圧を下げる目的で利尿薬が使われるのですが、大動脈弁狭窄症では、そうすると起立性低血圧(急に立ち上がったときに血圧が下がり、ふらつきやめまいを起こす)を引き起こす危険性があるからです。利尿薬で水分を排出し血液の量を減らすと、左心室から送り出す血液量も減ってしまうのです。
経カテーテル大動脈弁植え込み術「TAVI」とは?
大動脈弁狭窄症の治療法のひとつとして、最近、経カテーテル大動脈弁移植(あるいは留置)術(タビ:TAVI=Transcatheter Aortic Valve Implantation)が行なわれるようになってきました。経カテーテル大動脈弁置換術(タバ:TAVR=Transcatheter Aortic Valve Replacement)と言うこともあります。
胸をメスで切り開かず、心臓も止めずにカテーテルで弁の狭窄が改善できるので、体に優しい治療法として注目を浴びています。
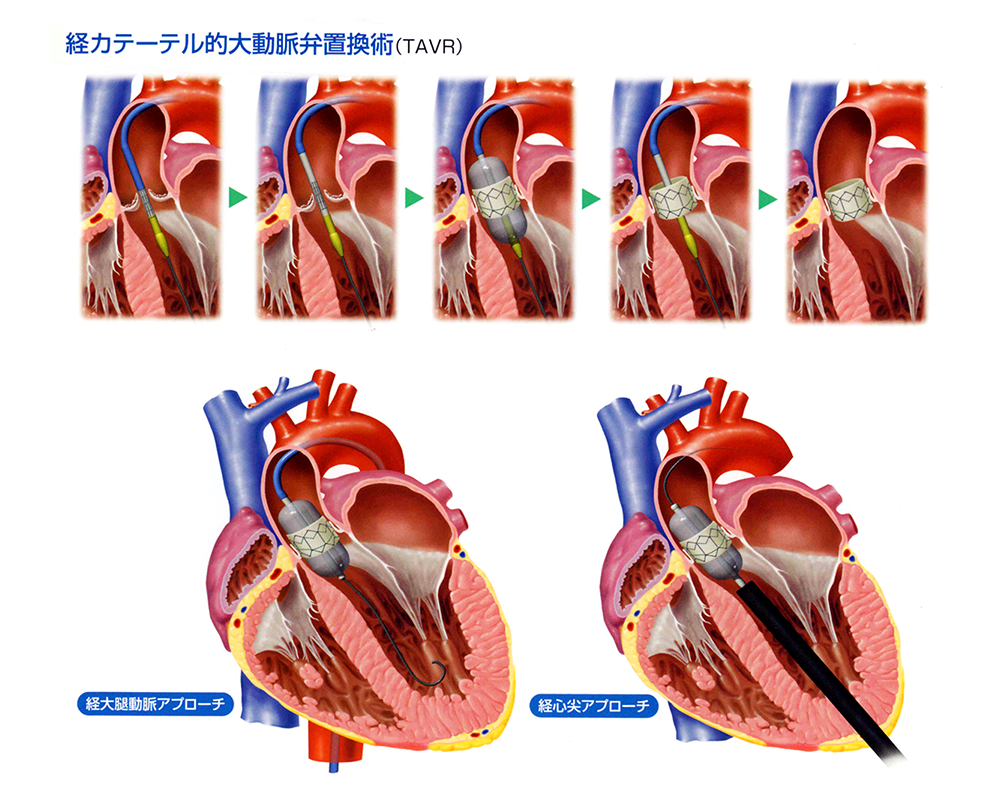
TAVIとは、以下のような治療法です。
まず、折り畳まれたバルーン(風船)と生体弁が装着されたカテーテルを、太腿の付け根などから動脈に挿入し、大動脈弁の場所まで持って行きます。ここで、まずバルーンを膨らませ、次いで生体弁を膨らませて留置します。こうすると、留置された生体弁が、狭窄している自己弁に代わって正常な弁機能を果たします(図7)。
低侵襲(体を傷つけにくい)という点では有効な治療法のひとつと言えますが、弱点があります。それは、カテーテルで置き換える弁が外科的に埋める弁よりも長持ちしないということです。
したがって、メリットがあるのは、外科手術に耐えがたい超高齢者や、さまざまな理由で外科手術が困難な患者さんに限られます。特に若い患者さんには、TAVIではなく、しっかりとした外科手術で弁を置き換えることをお勧めします。
経カテーテル大動脈弁留置術 - TAVI(タビ)についてはこちら
大動脈弁狭窄症の外科治療
大動脈弁狭窄症の外科治療には、損なわれた弁を人工弁に置き換える弁置換術と、自分自身の弁を修復する弁形成術があります。
①大動脈弁置換術
①-1:長所と短所
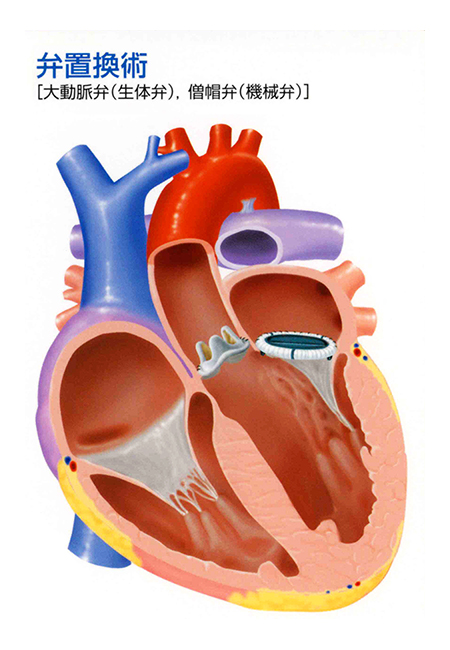
置換術で用いられる人工弁には、特殊なカーボン材で作られた機械弁と、牛の心膜や豚の大動脈弁を加工した生体弁があります(図8、9)。
機械弁の長所は半永久的な寿命があること、短所は弁の周辺で血液が凝固しやすいことです。この短所があるために、機械弁に置き換えたあとは、血液を凝固させないよう、抗凝固剤(ワーファリンなど)を一生飲み続けることになります。
生体弁の長所はそうした血液凝固の心配がないこと(ただし、手術後3~6か月くらいは抗凝固剤を服用する必要があります)、短所は機械弁ほど長持ちしないことです。一般に寿命は15年から20年程度です。若い人だと10年以下で石灰化などを起こし劣化します。劣化したときには再手術が必要になるので、若い人には生体弁は勧められません。
①-2:手術時間
大動脈弁の手術では心臓を一時的に薬で止めますが、心停止時間が長くなるほど心筋に与えるダメージが大きく、手術後の合併症も増えます。したがって、手術にはスピードと正確さが求められます。
弁置換術における心停止時間の全国平均は約97分ですが(日本胸部外科学会のデータによる)、ニューハート・ワタナベ国際病院では、人工弁の縫合技術を見直して、心停止時間を30~50分に大幅短縮しました。また、心臓を停止する液の組成・投与法を改善し、安全に心停止下の手術が行なえるようにしました。
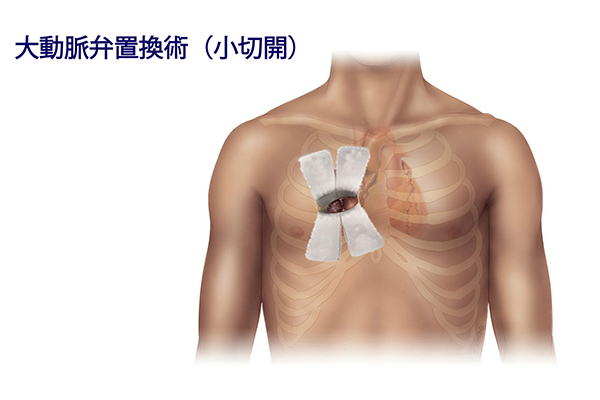
ニューハート・ワタナベ国際病院では、大動脈弁置換術の手術は、皮膚を切ってから閉じるまで大体2時間で終了します。大動脈弁の置換のみであれば、小切開手術(ミックス:MICS=minimally invasive cardiac surgery)を基本としています。
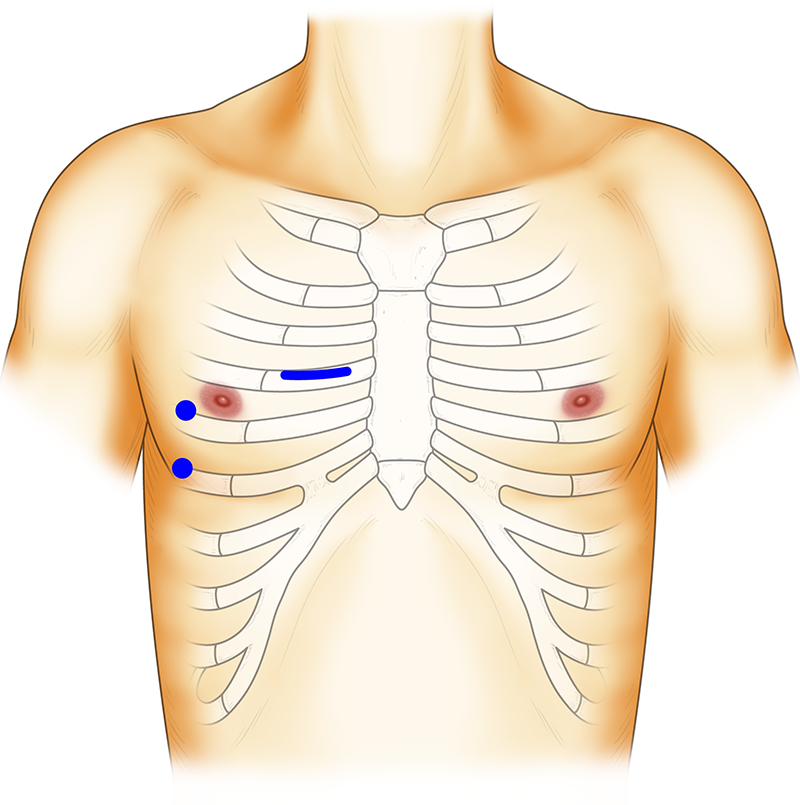
小切開手術とは、胸を大きく切り開かず、肋骨の下を6~8センチほど切り開いて行なう手術です(図10)。これを用いると、出血が少なく、手術後の回復も早いなど、患者さんの体の負担が大幅に改善されるだけでなく、入院期間も短縮され、手術の傷も目立ちません。MICSの和訳は「低侵襲(体を傷つけることの少ない)心臓手術」です。
②大動脈弁形成術
②-1:自己心膜を使う形成術とは?
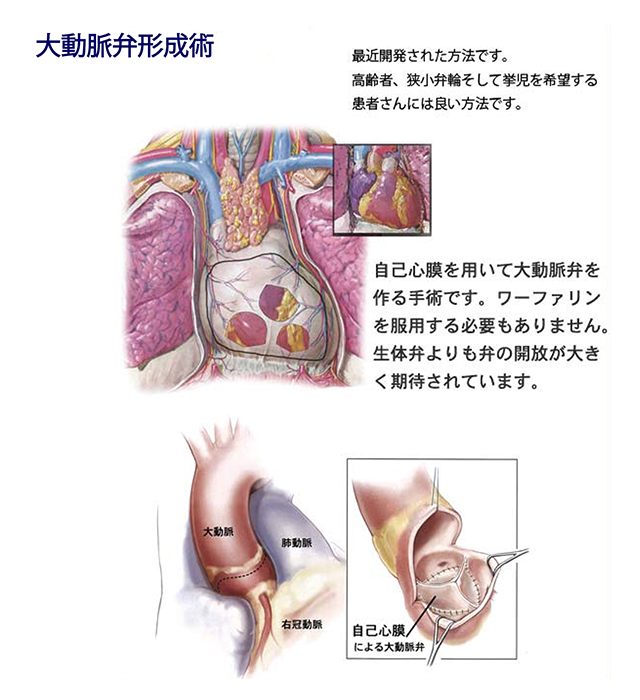
一般に大動脈弁形成術は、自分自身の弁を温存し、縫ったり繋いだりして修復する手術ですが、ニューハート・ワタナベ国際病院では、自己心膜(心臓を包んでいる自分自身の膜)を利用する方法をとっています(図11)。
自己心膜を切り取り、特殊な保護液で固定したあとに新たな弁尖を作成し、それを大動脈弁の位置に縫い付けるやり方なので、形成術というよりは、作成術と言ったほうがいいかもしれません。
東邦大学医療センター大橋病院の尾崎重之教授が考案したもので、新しい技術なので長期にわたる耐久性は不明ですが、尾崎教授は、弁は10年の経過観察で90%近い患者さんで再手術することなく機能している、と報告しています。生体弁よりも弁が大きく開放し、生体弁と同等以上の成績が期待されています。
②-2:自己心膜を使う利点、手術時間
自己心膜を使う大動脈弁形成術は、弁置換術に比べると、より生理的であるという利点があり、高齢者、弁輪(弁の外周)が小さく通常の人工弁に置き換えられない人、出産を希望する女性などに適しています。また、弁置換術と違い、血液を固まりにくくする薬(抗凝固剤)を服用する必要がないことも、この手術法の長所と言えます。
手術時間は、自己心膜を採取する必要から胸を大きく切り開かねばならず、3時間から3時間半です。
ただし、自己心膜を使う大動脈弁形成術は、弁置換術より難しく、執刀医によって技術力に大きな開きがあります。そのため、この手術を行なっている病院は、まだそれほど多くはありません。したがって、この手術を希望される方は、信頼するに足る外科医を慎重に選ばれるほうがいいでしょう。
人工弁と弁形成術の長所と短所の比較
大動脈弁手術における機械弁、生体弁、弁形成術の長所と短所を別表(表2)にまとめました。
| 抗血栓症 | 抗感染症 | 簡単な入手 | 血行動態 | 壊れにくさ(耐久性) | |
|---|---|---|---|---|---|
| 機械弁 | × | △ | ◎ | ○ | ◎ |
| 生体弁 | ◎ | △ | ◎ | ○ | △~○ |
| 弁形成 | ◎ | ◎ | ◎ | ◎ | △~○ |
大動脈弁手術の成功率
日本胸部外科学会が全国集計した2014年の公式データによると、単独大動脈弁手術における成功率は以下のようになっています。
弁膜症手術全般(再手術を除く)での病院死亡率は約3.1%(術後院内30日以内死亡は約1.9%)です。
透析治療と大動脈弁狭窄症の進行について
透析患者さんにおいては弁の石灰化は臨床上、重要な問題です。進行抑制を考えることが大事なのですが、腎機能が悪化した患者さんではリンなどのミネラルの代謝異常が重要な危険因子となります。
透析治療を受けている患者さんの大動脈弁口面積は、通常の大動脈弁狭窄症の患者さんに比べてその縮小するスピードが速く、大動脈弁口面積が0.9㎠になると半年程度で急速に予後が悪くなることが知られています。そのため、重症の大動脈弁狭窄症の方の弁口面積が、超音波検査などで0.9ないしは1㎠以下となった場合には、早急に手術を予定する必要が出てきます。
現在、TAVI(タビ:経カテーテル的大動脈弁置換術)というカテーテル治療もありますが、生体弁しか入れることのできないTAVIは極めて不利です。その理由は、透析患者さんでは生体弁の持ちが悪いからです。透析患者さん以外のカテーテル治療も6年程度と短いため、透析患者さんにとってはさらに短いことが予想されます。緊急的にであれば良いのですが、人生100年時代にはそうもいきません。できるだけ機械弁を入れるケースが出てくるものと思いますが、機械弁はカテーテル治療ができないために外科治療となります。
当院では、透析患者さんには安全な外科治療を受けることをお勧めしております。
子供の大動脈弁狭窄症手術
子供も大動脈弁狭窄症を発症することがあります。先天性の大動脈二尖弁は、生まれてくる子供の2%前後に出現すると言われており、小児期に大動脈弁狭窄症を発症するのはその一部です。重症例では、新生児期・胎児期から重症心不全が現われます。
ただ、心臓病を持って生まれてくる子供の多くは、成長と共に自然治癒したり、定期的な通院で経過を観察しつつ成人し、自立した生活を送れるようになったりします。女性の約9割は妊娠・出産も可能になります。
不幸にして発症した場合は手術となりますが、その場合には注意すべき点があります。それは、子供は成長するということです。成長して体が大きくなっても、その影響を弱めるよう、極力自己弁を温存したり、大きめの人工弁を使ったりといった、さまざまな工夫が求められます。やむをえず小さな、あるいは劣化する人工弁を使用した場合は、成長後、再手術が必要になることがあります。
小児ならではの難点や、小児に特有の手術法もあり、大動脈弁狭窄症のお子さんを抱えた方は、小児の心臓病を専門とする医師に相談するのがいいでしょう。
高齢者の大動脈弁狭窄症手術
70代、80代という高齢の大動脈弁狭窄症患者が増加しています。高齢化社会を迎え、多くの高齢者で加齢による弁の変性と動脈硬化が進行するためとされていますが、手術前に左室機能が大きく低下していた例、超高齢であった例、虚血性心疾患も合併していて冠動脈バイパスを同時に行なった例、NIHA[ニーハ]分類(慢性心不全の評価基準)が重症(Ⅳ度)であった例では、手術死亡率が高いという報告があります。
高齢者の手術については、身体活動度、精神状態、一般的なQOL(生活の質)、手術のリスクと術後の予後などを慎重に考慮する必要があります。年齢と実際の身体状況が一致しないときは、身体状況を重視すべきでしょう。術後の入院生活で下肢の筋肉が萎縮し、寝たきりになるケースも珍しくありません。
手術後
ニューハート・ワタナベ国際病院では、大動脈弁狭窄症の手術日および翌日は、HCU(重症治療室)に入り、点滴やドレーン(廃液管)が外れれば、次の日から歩行とリハビリができるようになります。
食事は手術の翌朝から可能です。手術から退院までは10~14日です。退院から職場復帰までは、デスクワークであればほぼ2週間、肉体労働であれば約1か月です。胸を大きく切り開く手術(正中[せいちゅう]切開手術)を受けた場合は、切った胸骨が元のようにくっつくまで、約2か月は安静にする必要があります。
予後
一般に大動脈弁狭窄症は予後が不良です。大動脈弁狭窄症の自然歴では、重症な自覚症状が出現してから突然死などで死亡するまでの期間は短く、心不全では2年、失神では3年、狭心症では5年で亡くなると言われています(図12)。
80歳以上の高齢者の場合、手術を拒否した症例の1年生存率は52%、2年生存率は40%、手術を受けた症例の1年生存率は87%、2年生存率は78%という報告があります。
症状のセルフチェックシート
まとめ
大動脈弁狭窄症は、発症しても無症状の期間が長く、症状が現われるようになったら予後が不良で、突然死の危険もあるという厄介な病気です。
日頃から高血圧や糖尿病、高脂血症などの動脈硬化を呼ぶ因子に気をつけるだけでなく、健康診断などで大動脈弁狭窄症の疑いが指摘されたり、階段を上ると息が切れるようになったりしたら、早めに医師の診断を仰ぎましょう。症状が出たら、なるべく早く手術を受けるようにしましょう。
関連記事
大動脈弁狭窄症に関するよくあるご質問
ニューハート・ワタナベ国際病院の心臓血管外科についてはこちらをご覧ください。