僧帽弁閉鎖不全症とは
僧帽弁閉鎖不全症とは、心臓の弁のひとつが正常に働かなくなって、心臓の中で血液が逆流する病気です。
さらに、社会の高齢化に伴って増加している心臓弁膜症の一つでもあります。
心臓や肺に負担をかけ、全身に充分な血液が送り出せず、息切れや咳、呼吸困難などが起こります。病勢が進むと心不全を引き起こしますが、慢性の場合、初期には自覚症状がなく、健康診断を受けたり、他の病気で検査をしたりしたとき、初めて気づくことがしばしばあります。
ここでは発症する原因、現われる症状、さらにその治療法などを説明します。
目次
僧帽弁閉鎖不全症とはどんな病気?
僧帽弁閉鎖不全症とは、心臓の弁のひとつである僧帽弁がきちんと閉じなくなる病気です。
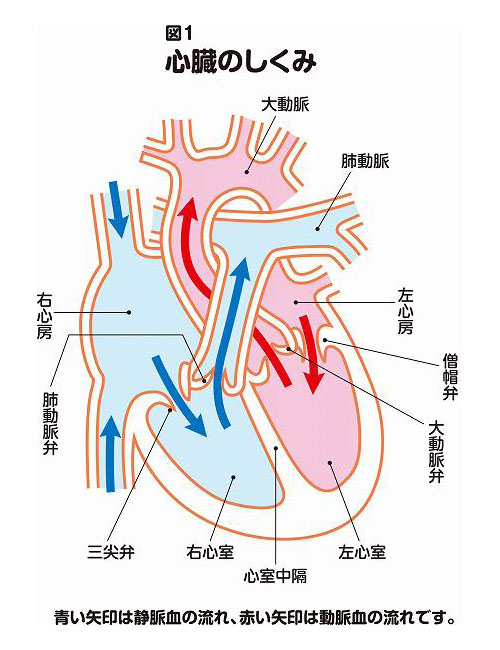
心臓には、血流をコントロールする4つの弁(三尖弁、肺動脈弁、僧帽弁、大動脈弁)があります。そのうちの僧帽弁と大動脈弁が果たしているのは、肺から心臓に届く酸素の豊富な血液(動脈血)を全身に送り出す際のゲートとしての役割です(図1 心臓のしくみ)。
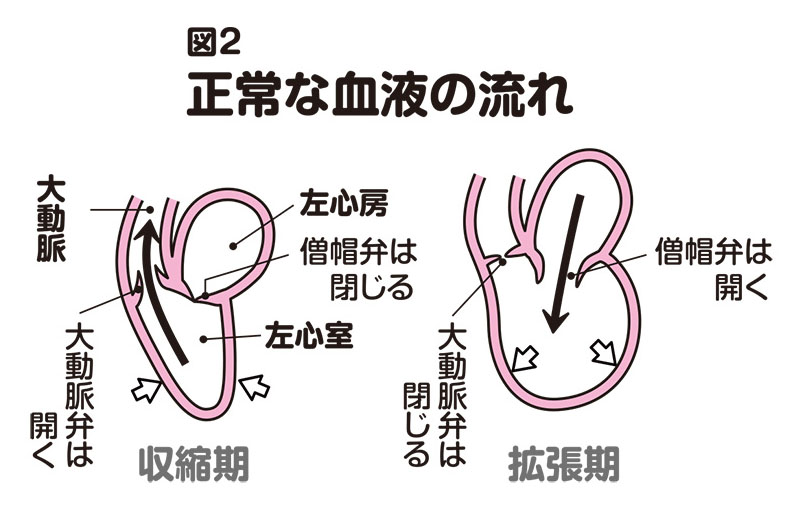
心臓が収縮すると僧帽弁が閉じて大動脈弁が開き、左心室から大動脈へ血液が送り出され、拡張すると僧帽弁が開いて大動脈弁が閉じ、肺と左心房から左心室に血液が送り込まれます(図2 正常な血液の流れ)。
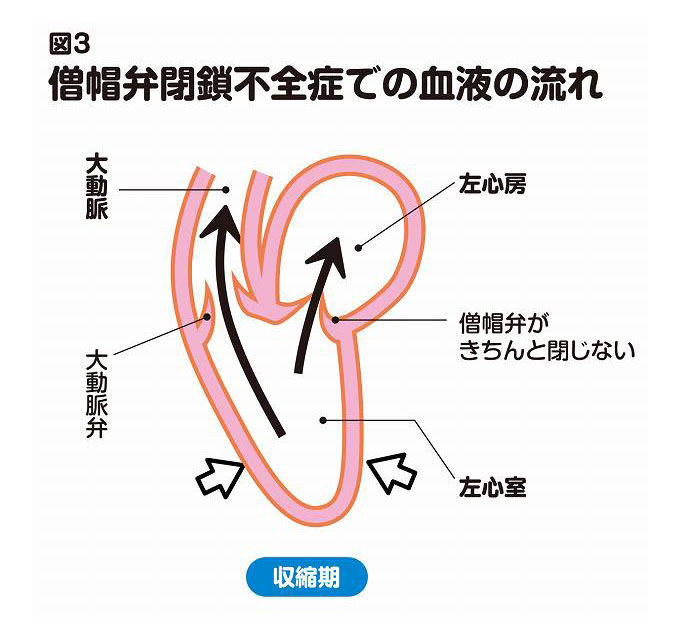
ところが、なんらかの原因で心臓の収縮期に僧帽弁がきちんと閉じなくなると、左心室に送った血液の一部が左心房に逆流するようになります(図3 正常でない血液の流れ)。これが僧帽弁閉鎖不全症です。
逆流が起こると、左心房・左心室ともに大きな負担がかかって肥大し、心臓から大動脈に送り出される血液の量が減り、肺も損なって息切れや咳、呼吸困難などが生じます。
僧帽弁閉鎖不全症と僧帽弁狭窄症の違い
僧帽弁閉鎖不全症と同様に僧帽弁に不具合を起こす病気に、僧帽弁狭窄症があります。こちらは、本来、僧帽弁がきちんと開くはずの拡張期に、弁が充分には開かなくなります。弁が狭窄して、左心房から左心室へ向かう血液が通りにくくなるのです。
このため、僧帽弁閉鎖不全症と同じように、息切れや咳、呼吸困難などが生じます。
僧帽弁閉鎖不全症と心不全の関係
僧帽弁閉鎖不全症になると、心不全を引き起こす危険性が高まります。心不全とは、心臓の機能が低下した状態です。
左心房への血液の逆流が起こると、左心房にも左心室にも大きな負担がかかりますが、病気の進み方が緩慢(慢性)であるか急速(急性)であるかによって、心不全の起こり方が変わってきます。
慢性僧帽弁閉鎖不全症における心不全
左心房への逆流が起こると、左心房の壁を拡大しようとする力が働きます。また、左心室から大動脈に送り出される血液の量が減るので、左心室はより強く収縮しようとし、やはり心室の壁を拡大します。
ただし、少しずつ徐々に拡大する場合(慢性の経過をたどる場合)は、左心房も左心室も、その状態でなんとか持ちこたえ、機能を維持しようとするので(こうした対応を「代償機構が働く」と言います)、しばらくは何の症状も現われません。
しかし、やがて持ちこたえきれなくなると、左心房の圧が上がり、左心室の収縮力も落ちて大動脈に送り出される血液の量が減り、その結果、肺に水が溜まったり(肺水腫)、うっ血(鬱血)したり(肺うっ血)、肺動脈(全身から戻ってくる二酸化炭素を多く含む静脈血を、右心室から肺に送る血管)の圧が高まったりして(肺高血圧症)、息切れや咳、呼吸困難などが生じ、左[さ]心不全を起こします。また、重症化して心房細動(心房が細かく震える不整脈)が起こると、動悸を感じたりします。
さらに、肺高血圧症により右心室の圧が上昇し、上下大静脈がうっ血するに至ると、浮腫[ふしゅ](むくみ)や肝腫大[かんしゅだい](肝臓が腫れた状態)などの右[う]心不全の症状が現われます。
急性僧帽弁閉鎖不全症における心不全
急性の場合は、急に生じた逆流に対応できず、左心房や左心室で代償機構が働く間もなく(壁を拡張する間もなく)、急速に左心房の圧が高まって肺うっ血や肺水腫をきたし、左心室から大動脈へ送る血液の量が減って、急激な心不全を起こします。ときにはショック状態となることもあります。
原因
原因を説明する前に、前提の知識として、弁の構造を解説します。
僧帽弁の構造
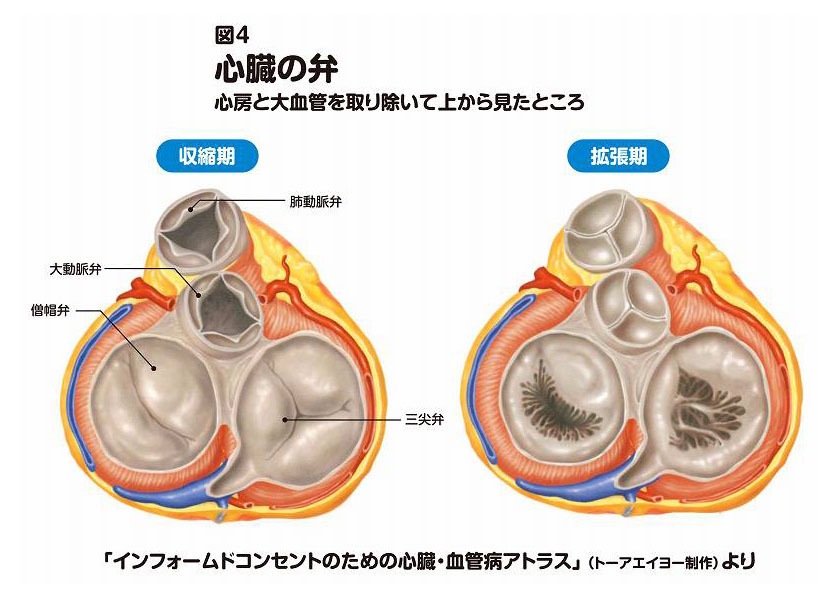
他の3つの心臓の弁(大動脈弁、三尖弁、肺動脈弁)は3つの弁尖[べんせん](弁尖とは、弁を開閉する扉の役割を果たす膜の部分)から成っていますが、僧帽弁のみは、大きめの前尖と、小さめの後尖の2つの弁尖から成っています(図4 心臓の弁)。
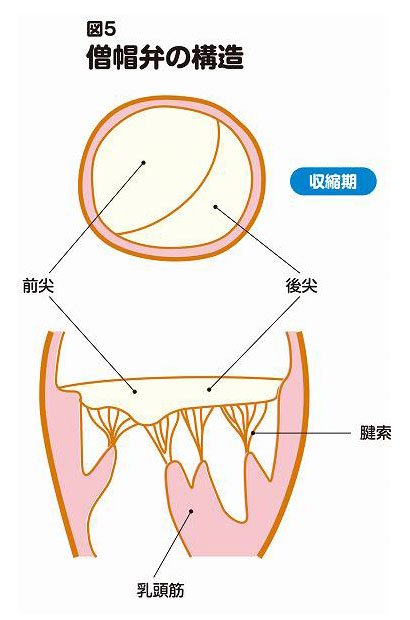
僧帽弁の弁尖には、左心室側から伸びる腱索[けんさく](ひも状のもの)が付いていて、その腱索は左心室壁の乳頭筋[にゅうとうきん]から伸びています(図5 増帽弁の構造)。
心臓(心室)の拡張期には、僧帽弁の弁尖が乳頭筋と腱索に引っ張られることで左心室側に開き、左心房から血液が左心室に流れ込みます。一方、収縮期には、前尖と後尖がぴたりと合わさることで弁が閉じ、左心房からの血流を止めます。このとき前尖や後尖は、腱索に繋がっているために、左心房側にははみ出しません(反転しません)。
なお、僧帽弁という名前は、弁の外観が仏教やキリスト教の偉いお坊さんが被る帽子の形に似ていることから付けられた、と言われています。
僧帽弁の壊れ方
【前尖や後尖の異常】
前尖や後尖が、裂けたり穴が開いたりといった変性をきたします。
【腱索や乳頭筋の異常】
何らかの理由で腱索が切れたり伸びたり、乳頭筋が傷んだりする事態です。その結果、前尖や後尖が左心房側にはみ出すことがあります(このはみ出した状態を「逸脱」と言います)。
【弁輪の拡張】
弁輪というのは弁の外周部分で、径が広がり弁輪が拡張すると、きちんと閉じなくなります。
僧帽弁が壊れる原因
原因としては、粘液様変性、リウマチ熱の後遺症、感染性心内膜炎、バーロー症候群(Barlow’s syndrome)やマルファン(Marfan)症候群などの先天的な(生まれつきの)疾患、心筋症、虚血性心疾患などが考えられます。
【粘液様変性】
なんらかの理由で細胞が多量の粘液物質を産生することが原因となって弁尖が変性をきたし、左心房側に逸脱します。
【リウマチ熱の後遺症】
リウマチ熱は、溶連菌(溶血性連鎖球菌)による咽頭炎が引き起こす全身性の自己免疫疾患で、発熱や関節炎などを起こすだけでなく、心筋の組織も侵し、しばしば僧帽弁に炎症を引き起こします。リウマチ熱のほとんどは、小児期にかかると言われていますが、近年は抗菌薬の普及や衛生環境の向上もあり、先進国では減少傾向にあります。
一方、発展途上国では抗菌薬が使用されなかったりするため、抗菌薬の恩恵を受けられなかった高齢者では、現在もリウマチ熱が僧帽弁閉鎖不全症の原因となっています。
【感染性心内膜炎】
感染性心内膜炎とは、細菌(主にグラム陽性細菌)が引き起こす心臓組織の炎症です。なんらかの原因で傷ついた心内膜にフィブリン(血液の凝固にかかわる繊維状タンパク質)と血小板が沈着し、そこに細菌が付着してイボ状のできもの(疣腫[ゆうしゅ])を形成します。これが弁尖にできると、弁尖に穴を開けたり、弁尖を引っ張る腱索を断裂させたりします。
抜歯などの歯科治療をきっかけに細菌感染することが多いので、弁に問題を抱えている人で歯科治療が必要な人は、歯科医とよく相談し、歯の治療後、抗生物質を服用したほうがいいでしょう。
【バーロー症候群】
生まれつき僧帽弁がふやけたような柔らかい形状をしている病気で、前尖も後尖も著しく肥厚し、逸脱します。
【マルファン症候群】
マルファン症候群とは、遺伝子の異常により組織と組織を繋ぐ結合組織が弱くなって、全身で細胞の弾力性がなくなる病気です。血管壁を弱体化させ、心臓の弁を壊します。マルファン症候群では30代で亡くなるケースが稀ではなく、その死因の大半は、解離性大動脈瘤などの心臓や血管の疾患と言われています。
【心筋症】
心筋症とは心筋(心臓の筋肉)が何らかの原因で損なわれた状態で、左心室で心筋症が起こると、結果として、二次的に僧帽弁閉鎖不全を引き起こすことがあります。
【虚血性心疾患】
狭心症や心筋梗塞で心筋に血液が届かなくなると、乳頭筋にも血液が行かなくなって断裂することがあるほか、心筋梗塞や心不全で左心室が拡大し、二次的に左心房への逆流が生じる場合があります。左心室の拡大に伴って逆流弁口が広がり、逆流量が増大して病態をさらに悪化させることもあります。
心臓の弁の疾患は、生活習慣病や加齢が原因となることも多く、一般に年配者の病気と思われがちですが、若年層にも決して無縁ではなく、リウマチ熱の後遺症や、先天性のバーロー症候群やマルファン症候群などにより発症することがあります。
症状
初期は、多くの人が無症状で経過しますが、進行して心臓や肺に負担がかかるようになると、さまざまな症状を呈するようになります。
まず現われるのは肺の症状で、階段や坂道の上り下りで息切れを起こします。病勢が進むと、平らな道を歩いたり、着替えなどの軽い動作をしたりしても、息切れを起こすようになります。夜間に小水に起きるのも心不全の症状の一歩です。
さらに進むと、安静時や夜寝ているときに急に呼吸が苦しくなったり(夜間発作性呼吸困難)、横になっただけで息苦しく、常に体を起こした姿勢でいるしかなくなったりします(この状態を「起坐[きざ]呼吸」と言います)。なぜ寝ている姿勢より起きている姿勢のほうが呼吸が楽なのかというと、体を横(水平)にすると、下半身に行っていた血液が急に心臓に戻り、肺うっ血が強まるからです。
重症になると、激しく咳込み、ピンク色の痰を出すようにもなります。胸が痛むこともあり、胸痛が出てから、狭心症ではないかと疑って受診する人もいます。肺炎とよく間違えられることもあります。
心房細動が出たら要注意
進行例では、心房が細かく震える、心房細動という不整脈を高頻度で合併します。心房細動が起こると、動悸や胸部不快感、胸痛、立ちくらみ(めまい)、全身倦怠感が生じます。
心房細動には、脳梗塞を引き起こす危険性があります。心房細動によって心房内に血栓(血の塊)が形成され、その血栓が大動脈を経由して脳の血管に飛び、塞いでしまうことがあるからです。そのため、症状の出ていない僧帽弁閉鎖不全症であっても、心房細動が生じている場合は、手術を検討することがあります。
心音
僧帽弁閉鎖不全症では、症状が現われる前から、聴診で心臓からの特有の雑音が聞こえます。
心音(心臓から出てくる音)は、正常なら、房室弁(三尖弁と僧帽弁)の閉鎖で生ずるⅠ音と、心室収縮期の終了時に動脈弁(大動脈弁と肺動脈弁)の閉鎖で生ずるⅡ音が聞こえますが、弁尖が逸脱していると、心室収縮期(つまり逆流が生じている時期)の全般にわたって、高い調子の著しい雑音が生じるのです。
ただし、虚血性や拡張型心筋症などによる僧帽弁閉鎖不全症の場合には、逆流ジェットが強くなく、雑音が聞こえないケースもあります。
心電図
心電図とは、心臓の電気的活動をグラフ化したものです。
僧帽弁閉鎖不全症では左心房・左心室に負荷がかかりますが、その様子が心電図からうかがえます。
進行例には、心房細動が高頻度で合併しますが、心電図では、心房細動が起こっているかどうかも確認できます。
検査・診断方法
心電図以外の検査としては、以下のようなものがあります。
経胸壁心エコー検査
胸の表面(胸壁)から人間の耳に聞こえない超音波(エコー)を当てて心臓の内部を探る検査で、体に負担がなく、ベッドサイドで簡便に行なえます。この検査で、弁自体の性状(大きさ、長さ、石灰化などの硬さ)、逸脱の有無、逆流の向きや程度、逆流する血液の割合、逆流口の大きさ、左心室の収縮する力、左心室の大きさなど、多岐にわたる情報が得られ、それらを統合して原因や重症度を判断します。確定診断に必須の検査です。
経食道心エコー検査
通常の経胸壁心エコー検査では弁の状態が見えにくい場合は、経食道心エコー検査を行なうことがあります。これは、胃カメラのような太い超音波プローベ(探触子)を口から食道に飲み込むことで、心臓の裏側から直接、弁の観察を行なうものです。僧帽弁は胸の奥のほうにあって見えにくいのですが、この検査を行なうと、より詳細な情報が得られます。
胸部エックス線検査
エックス線撮影により心臓の状態を探る検査です。心臓がどの程度拡大しているか、逆流はどの程度か、といったことが分かります。ただし、心臓の拍動のリズムが保たれている場合は、拡大が顕著ではないこともあります。
心臓カテーテル検査(左室造影検査)
大動脈に挿入したカテーテルを使い、大動脈と心臓に造影剤を流してエックス線撮影をすることで、僧帽弁からの逆流の程度を調べる検査です。入院した上での検査になります。最近では、心エコー(超音波)検査で分かるので、左室造影はほとんど行ないません。
血液検査
主に心室から分泌され心筋を保護する働きをする、BNP(脳性ナトリウム利尿ペプチド)というホルモンがあります。BNPは心臓に負担がかかったり、心筋が肥大したりすると血中濃度を増します。自覚症状が出る前から濃度が上がるので、心機能低下の早期発見に役立ちます。
心エコー(超音波)検査の重症度分類・レベル
重症度は心エコー(超音波)検査で判定します。
定性評価法と定量評価法とがあり、それぞれ軽度(mild)、中等度(moderate)、重度(severe)の3段階で評価します(表1)。これに微少(trivial)を加え、4段階で評価することもあります。
| 軽度(mild) | 中等度(moderate) | 重度(severe) | |
|---|---|---|---|
| 定性評価法 | |||
| カラードプラジェット面積 | 左房面積の20% | 左房面積の20~40% | >左房面積の40% |
| Vena contracta幅 | <0.3cm | 0.3~0.69cm | ≧0.7cm |
| 肺静脈血流シグナル | 収縮期波優位 | 収縮期波減高 | 収縮期逆行性波 |
| 定量評価法 | |||
| 僧帽弁逆流量 | <30mL | 30~59mL | ≧60mL |
| 僧帽弁逆流率 | <30% | 30~49% | ≧50% |
| 有効逆流弁口面積 | <0.20cm2 | 0.20~0.39cm2 | ≧0.40cm2 |
表1 僧帽弁逆流の重症度評価
定性評価法
カラードプラジェット面積、Vena contracta幅、肺静脈血流シグナルの3つの項目で評価します。
・カラードプラジェット面積
心エコー検査のひとつであるカラードプラ法で逆流ジェットの面積を測定するものです。面積が広いほど重症です。カラードプラ法では、心臓内の血流の方向と速度を測定することができます。探触子に近づく血流は赤く、遠ざかる血流は青く、速い血流は明るく、遅い血流は暗く表示し、赤青黄緑が混在するモザイクパターンは乱流を示します。
逆流が増すにつれ収縮期波の高さが次第に落ち、重症例では逆流波が肺静脈内に流入します。
定量評価法
僧帽弁逆流量、僧帽弁逆流率、有効逆流弁口面積の3つの項目で評価します。
・僧帽弁逆流量
僧帽弁から左心房へ逆流する血液の量を測定します。多いほど重症です。
・僧帽弁逆流率
僧帽弁から左心房へ逆流する血液の割合を測定します。高いほど重症です。
・有効逆流弁口面積
逆流する弁口の面積を測定します。広いほど重症です。
重症度が高度の人は外科手術が必須ですが、高度でなくても、心機能が低下していたり、心房細動が出現していたりする場合は、早めに手術を受けることをお勧めします。
なお、逆流の重症度と症状の重症度は一致しません。症状がなくても、逆流による心機能の低下が見られることがあります。
治療方法
軽度から中等度の場合
軽症の場合は、利尿薬や血管拡張薬などの薬による内科的治療を行ない、心臓の負担を減らす、不整脈を予防する、血栓を予防するなどの治療を行います。
ただし内科的治療は、あくまで進行を抑える対症療法であり、僧帽弁そのものを修復することはできません。
中等度~重度の場合
一般に、呼吸困難などの症状が出ていたり、心臓の負担が増していたり(左心室の収縮力の低下、左心室の拡大、心不全の出現)、心房細動が生じていたりする場合は、根治に向けた治療が必要で、その基本は手術です。超音波検査で重度の逆流が見られれば手術適応です。また、超音波検査の計測で逆流率が分かりますが、50%以上の逆流がある場合も同様です。
また、心房細動を合併している場合は、僧帽弁を修復するだけではなく、心房細動を抑える手術(メイズ手術など)も検討します。
治療(手術)方法
手術には、 主に弁を人工のものに置き換える方法 (弁置換術) と、 弁を温存し修復する方法 (弁形成術) の2つと、カテーテル治療があります。
弁形成術のほうが弁置換術より技術的に難しいのですが、最近の傾向として、まず弁形成術が可能かどうか検討する傾向にあります。手術死亡率の低下、左心室機能の回復、術後合併症(脳梗塞や感染症、血栓症など)の回避、再手術の回避など、多くの点で弁置換術より優れているからです。日本胸部外科学会の調査では、2013年の僧帽弁手術における弁形成術の割合は、平均60%です。ニューハート・ワタナベ国際病院では、リウマチ性弁膜症以外であれば、ほぼ100%が弁形成となります。
ちなみに、逆流が軽度の場合、特別な治療は必要ない場合がありますが、逆流は徐々に悪化する可能性があるため定期的にエコー検査などを受けて、手術が必要かどうかを見極めましょう。
弁置換術
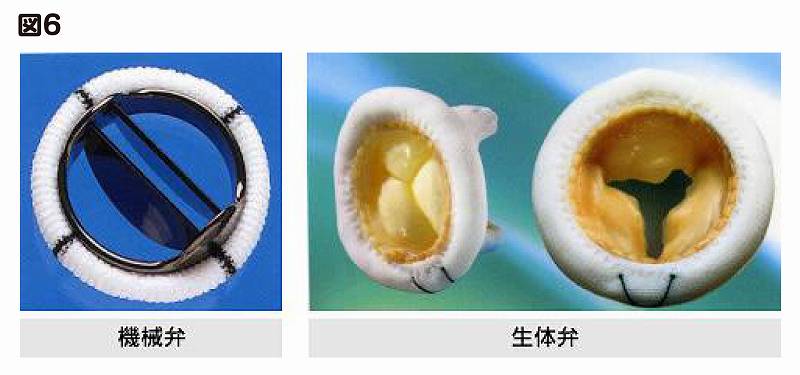
弁置換術では、弁を人工弁に置き換えます。人工弁には機械弁と生体弁があります(図6 機械弁と生体弁)。
機械弁は特殊なカーボン材でできていて、弁の寿命は半永久的です。ただし、弁の周辺に血液が凝固しやすいので、手術後、血を固めないための薬剤(抗凝固剤:ワーファリンなど)を毎日飲み続けなければなりません。
生体弁は牛の心膜や豚の大動脈弁を加工したもので、機械弁におけるような血液凝固の心配はありません(ただし、手術後3~6か月くらいは抗凝固剤を服用する必要があります)。問題は機械弁ほど長持ちしないことです。一般に、15年から20年程度(若い人だと10年以下)で劣化するので、そのときには再手術が必要になります。僧帽弁に生体弁を入れた場合には、大動脈弁のように長持ちはせず、10年経たないうちに壊れることをよく経験しています。
病変が弁形成術では修復困難な場合は、弁置換術が選択されます。
弁形成術
弁形成術では、自分の弁を温存し、縫ったり繋いだりすることで弁を修復します。自分の弁を修復するので弁の周辺での血液凝固がなく、置換術で機械弁に取り換えた場合のような抗凝固剤が不要です。
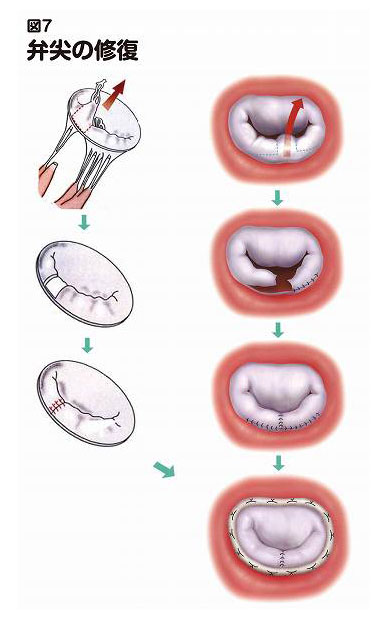
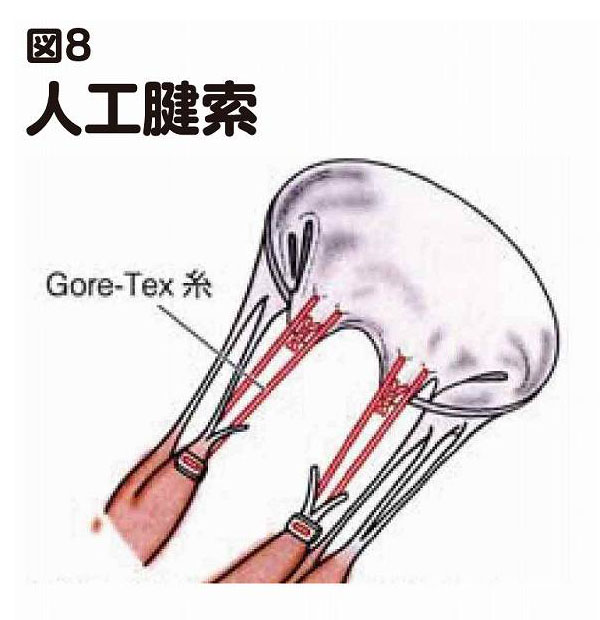
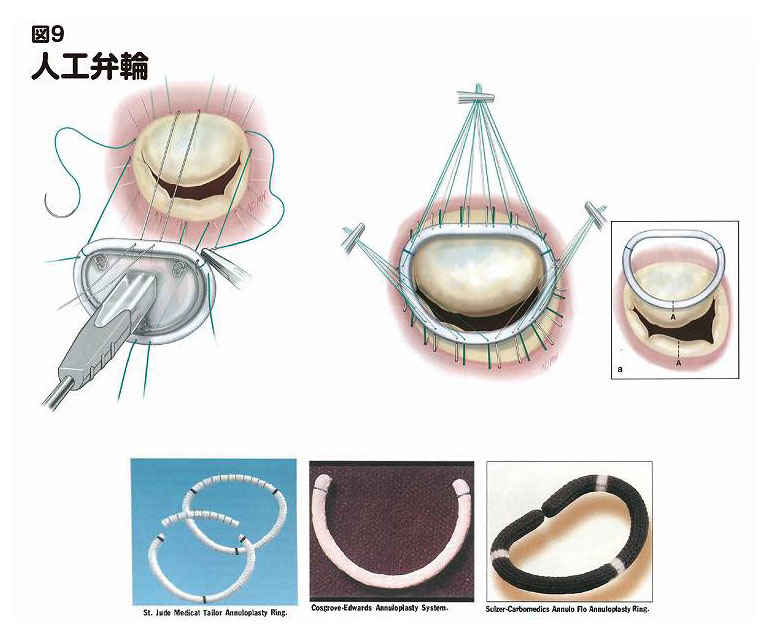
具体的な形成方法としては、逸脱部分を切除して縫い合わせたり(図7 弁尖の修復)、腱索を糸で再建したり(図8 人工腱索)、弁輪(弁の外周)が拡大している場合は、弁輪に糸をかけリング(人工弁輪)を縫い付けることで縮めたりします(図9 人工弁輪)。
弁形成術は、外科医によって技術力に大きな開きがあり、せっかく手術を受けながら(あるいは再手術を受けながら)、手術直後から再び逆流が生じてしまうケースが珍しくありません。手術を受ける場合は、症例数が多く、成績の良い施設を選ばれることをお勧めします。
ニューハート・ワタナベ国際病院では、僧帽弁のみの手術では、リウマチ性のものを除き、術前の検査で弁形成が可能と診断した場合、ほぼ100%弁形成術を行なっています。
僧帽弁閉鎖不全症のカテーテル治療
経皮的僧帽弁クリップ術 MitraClip®(マイトラクリップ)は、僧帽弁閉鎖不全症に対して、僧帽弁の逆流を軽減することを目的とした治療法の1つです。経皮的に治療を行うので傷口が小さく、また人工心肺を使わないため、身体への負担が少ない治療方法です。
保険適用で、ニューハート・ワタナベ国際病院の循環器内科でも、この治療方法を行っています。
手術における胸の切開の仕方
胸の切開の仕方には、胸骨正中[きょうこつせいちゅう]切開と低侵襲手術の2つがあります。低侵襲手術とは、極力体にメスを入れない体にやさしい方式です。
低侵襲手術には、ダビンチ手術(手術支援ロボット“ダビンチ(da Vinci Surgical System)”を用いた完全内視鏡下手術)とMICS(ミックス:ポートアクセス法)があります。
①胸骨正中切開手術
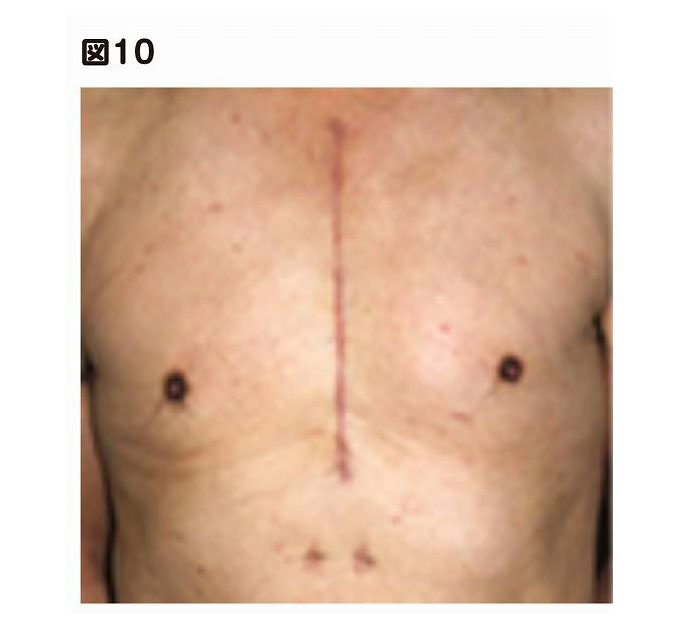
胸を喉からみぞおちのあたりにかけて縦に25~30センチくらい切り開き、開胸器で押し広げ、心臓を露出させて行ないます(図10 胸骨正中切開写真)。胸の真ん中正面には、縦に胸骨という大きな骨があり、そこから何本もの肋骨が横に張り出しています。心臓や肺は、この籠のような形をした骨の中に収められ、保護されています。そのため、僧帽弁を手術する際には、この胸骨を切り開き、押し広げることになります。
この手術には以下のような短所があります。
・胸を大きく切り開くので、痛みその他、患者の体に大きな負担がかかる。
・胸骨が元どおりくっつくまでに時間がかかり、それだけ入院も長期にわたり、社会復帰も遅れる。
・手術が原因の感染症が起こりやすい。
・大量の出血をする。
・不整脈や心不全を起こしやすい。
②低侵襲手術
胸骨正中切開の短所をカバーするために開発されたもので、患者さんの体の負担を極力軽くする小切開の方式です。
②-1:ダビンチ手術(ロボット手術)=超精密鍵穴(キーホール)心臓手術
手術支援ロボット“ダビンチ(da Vinci Surgical System)”を使う手術です。内視鏡を高度に進化させ、コンピュータ制御にしたものと言えるでしょう。
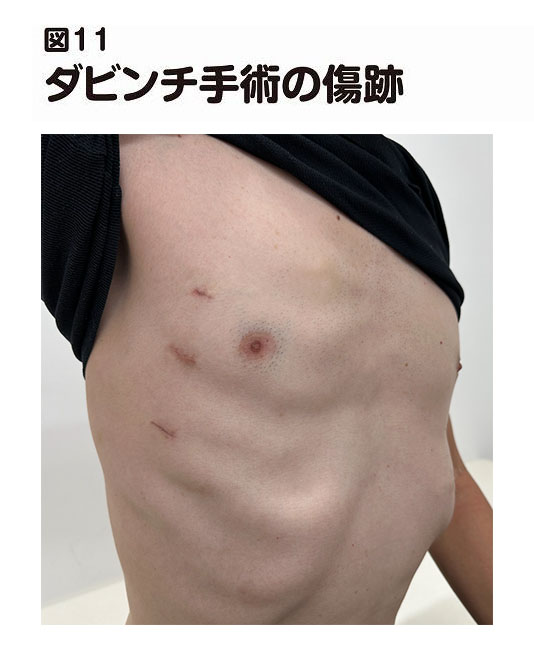
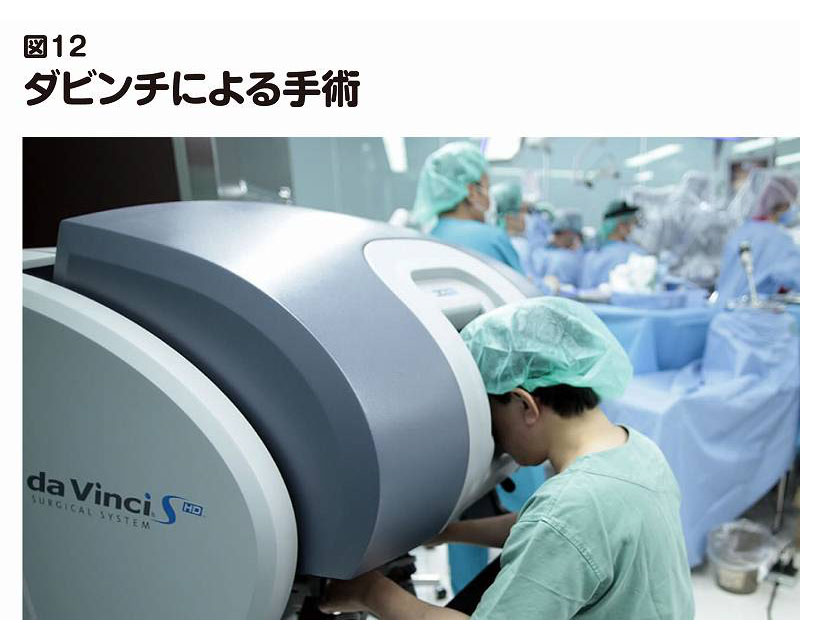
胸に3つの小さな穴を開け(図11 術後の傷跡)、そこからメスや鉗子[かんし]、カメラなどを装着したロボットの腕(アーム)を差し込みます。担当する医師は3メートルほど離れた操作台から、送られてくるモニター画像を見ながらロボットの腕を操作します(図12 ダビンチを操作中の写真)。3つの小さな穴を開けるだけなので、患者さんの負担は最も軽く、手術中の出血も極めて少なく、傷の痛みも少なく、神経も傷つけず、傷もすぐふさがって、手術後3日の入院で帰宅することも可能です。
特に僧帽弁に対する手術としては、ダビンチ手術は理想的な方式と言えます。胸骨正中切開では、僧帽弁は深く切り立った崖のようなところに位置していて、その閉鎖不全状態を観察するのがなかなか難しいのですが、ダビンチでは、右横からのアプローチなので、観察が容易です。モニター画像は3次元、操作はミリ単位なので、正確な弁形成が可能です。術後の弁機能はとてもよく保たれます。ただし、医師に高度の技術力・経験が求められます。
2018年4月から、ダビンチ手術を用いた弁形成術に健康保険が使えるようになりました。ニューハート・ワタナベ国際病院では、僧帽弁形成術の第一選択としてダビンチ手術を行なっています。
ダビンチ手術(ロボット手術)について詳しく知りたい方はこちらをご覧ください。
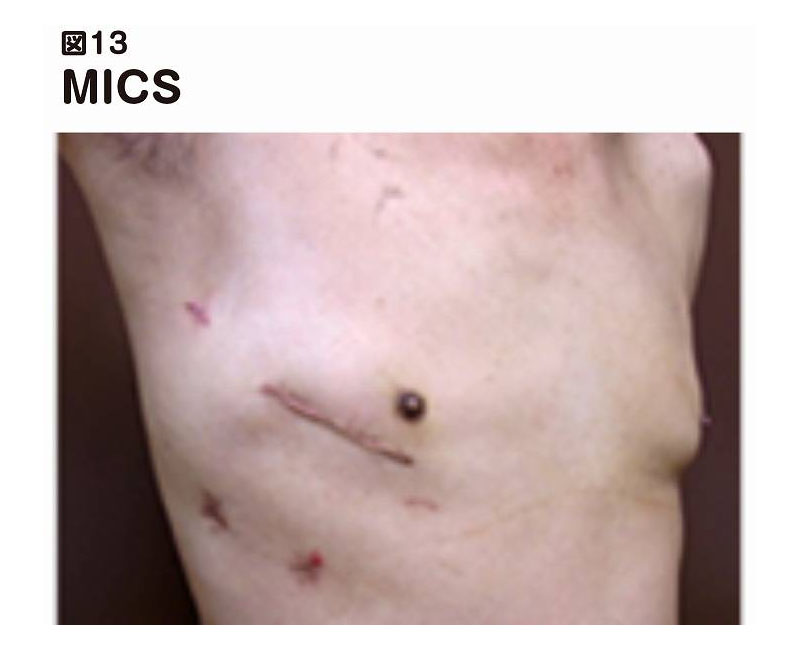
②-2:MICS(ミックス:minimally invasive cardiac surgery)
胸骨を切り開かず、右側の胸の肋骨の下を6~8センチほど切り開いて弁にアプローチする方式です(「ポートアクセス法」とも言います)(図13 MICS)。
胸骨正中切開に比べ、出血や痛みが少なく、傷も小さく、手術後の回復も早いなど、患者さんの体の負担が大幅に改善されます。また、入院期間も短縮され、手術の傷も目立ちません。術後2か月間の運動制限もほぼありません。
MICSの元々の英文を日本語に直すと「体を傷つけることの少ない(低侵襲の)心臓手術」になります。
ダビンチ手術同様、胸の右横からのアプローチなので、僧帽弁の閉鎖不全状態の観察が容易で、正確な弁形成ができます。
ニューハート・ワタナベ国際病院では、ダビンチ手術を選択しない場合の僧帽弁形成術は、ほぼこのMICSで行ないます。ダビンチでの内視鏡手術の技術が、MICSに応用されているわけです。
ダビンチ手術同様、MICSも、医師に極めて高度な技術力・経験が求められるほか、麻酔科医・臨床工学技士・看護師らとの緊密なチームワークが求められます。
なお、日本胸部外科学会が全国集計した公式データ(2014年)によると、弁膜症手術での病院死亡率は約3.7%(術後院内30日以内死亡は約2.2%)ですが、ニューハート・ワタナベ国際病院では0.3%です。
手術時間・入院日数・期間
ニューハート・ワタナベ国際病院におけるダビンチの手術時間は約2時間30分です。
また、手術後の患者さんの入院日数は、ニューハート・ワタナベ国際病院では、ダビンチ手術の場合で7〜8日、MICSなら8~14日です。退院後、自宅で1~2週間療養すれば、社会復帰が可能です。
手術後の生活
手術を受けたあとは、血圧を低めに管理し、心臓の負担を軽くする必要がありますが、そのほかにも、以下のような注意が必要です。
弁置換術を受けた人
機械弁に置換した患者さんは、機械弁に血栓が生じやすいため、生涯ワーファリンなどの抗凝固剤を服用しなければなりません。血栓が血液に乗って体の各部に運ばれると、そこで塞栓症を起こす危険があるからです。特に詰まりやすいのは脳、腹部、腎臓、手足などの血管です。
一方、抗凝固剤が効きすぎて、血が止まりにくくなることもあります。たとえば、胃潰瘍などの消化管出血、頭部打撲後の脳出血、歯茎からの出血や鼻血などが止まらなくなる事態です。そんなときは直ちに医師と相談してください。
生体弁に置換した人では、機械弁と比べ耐久性に劣るので、いずれ弁が壊れたり、変形したり、硬化したりすることが予想されます。したがって、定期的に通院し、経過観察を怠らないでください。
手術前に心機能が悪化していた人
手術前に心臓の機能が大幅に低下していた患者さんの中には、手術をしてもその回復が思わしくない人がいます。そうした人は、日常生活で以下のような注意が必要です。
・心臓に負担のかかる運動や作業を控える。
・水分や塩分の取り過ぎに気をつける。
・体にむくみが出ていないか気をつける。
・充分な睡眠をとり、疲れないようにする。
・風邪などをひかないようにする。
まとめ
僧帽弁閉鎖不全症は、心臓の中で血液が逆流する病気ですが、初期は自覚症状が無く、多くの人が進行し、呼吸困難などの心不全の症状が出て初めて気がつきます。
薬では治せず、完治しようとすれば手術するしかありませんが、幸いなことに、手術法は目覚ましい進歩を遂げています。ロボット支援のダビンチ手術やMICSなどの最先端の手術なら、体に優しく安全で、早期の社会復帰が可能です。
ただし、施設によって経験と技術力に大きな開きがあるので、その見極めが肝心です。
ニューハート・ワタナベ国際病院の心臓血管外科についてはこちらをご覧ください。