大動脈解離とは
大動脈解離とは、大動脈の血管壁が裂け、血液の通り道が、本来のものとは別にもうひとつできた状態です。
その結果、胸や背中に激痛が走り、大動脈が破裂したり、多くの臓器に障害をもたらしたりする重大な合併症を引き起こします。放置すると命にかかわります。
ここでは、大動脈解離はどういう原因で起こり、どんな症状が現われ、どう治療するのかなどについて説明します。
大動脈解離とはどんな病気?
大動脈解離とは、大動脈の血管壁になんらかの理由で亀裂が入り、そこから血管壁の中に血液が流れ込んで、本来の血液の流れ道とは別の、もうひとつの流れ道ができた状態です。この血管壁の裂けた状態を「解離」と呼びます。
大動脈の血管壁は、内膜・中膜・外膜の三層構造になっています。血液の流れる側が内膜、外側が外膜、内膜と外膜の間にあるのが中膜です。
内膜が裂けると、その裂け目から血液が中膜に流れ込み、中膜が膨らみます。この膨らみを「偽腔[ぎくう]」(解離腔)と言い、本来の血液の通り道を「真腔」と言います(図1)。
偽腔の外側には外膜しかないので、血圧に負けて外膜が破れ、血管の外に出血したら、致命的な事態を招くことになります。
偽腔は、血流の強い圧力に押され、血液の流れる方向に沿って、ある一定の長さに伸びてゆきます(つまり、解離が広がってゆきます)。偽腔を流れる血液は、流入した裂け目とは別の内膜の裂け目から、再び真腔に戻ります。真腔から偽腔への血液の入り口を「エントリー(流入口)」、偽腔から真腔への血液の戻り口を「リエントリー(流出口)」と呼びます。真腔と偽腔を隔てる血管壁(内膜・中膜)を「フラップ」と呼びます。
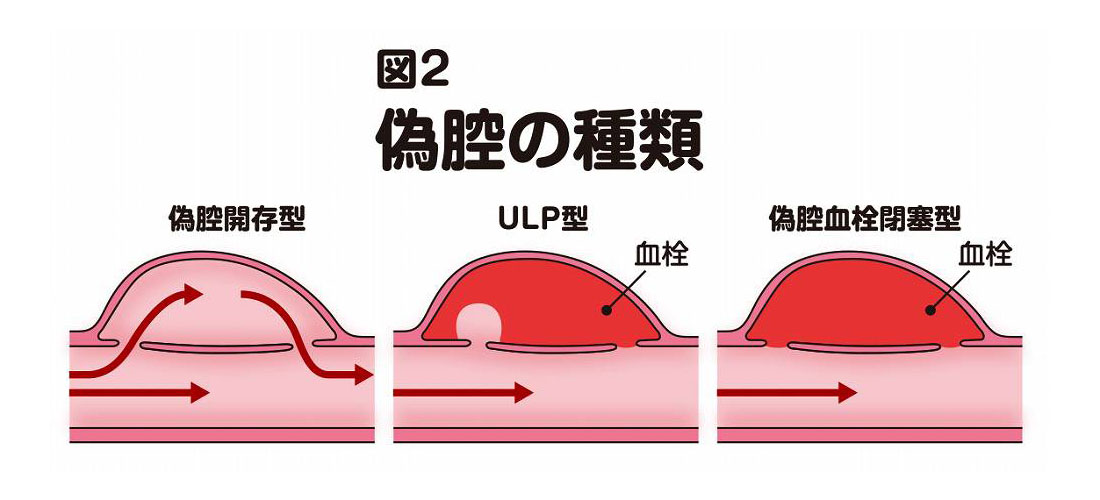
偽腔の種類
偽腔には3つのタイプがあります(図2)。
【偽腔開存型】
エントリーから流入した血液がリエントリーから流出しているタイプで、偽腔の中に血流がある状態です。
【ULP型】
エントリーから偽腔に突出する血流(これをULPと呼びます)は確認できるけれども、流入した血液はリエントリーから流出せず、ほとんどが血栓(血の塊)となっているタイプです。
【偽腔血栓閉塞型】
偽腔が血栓で完全に塞がっていて、血流がないタイプです。
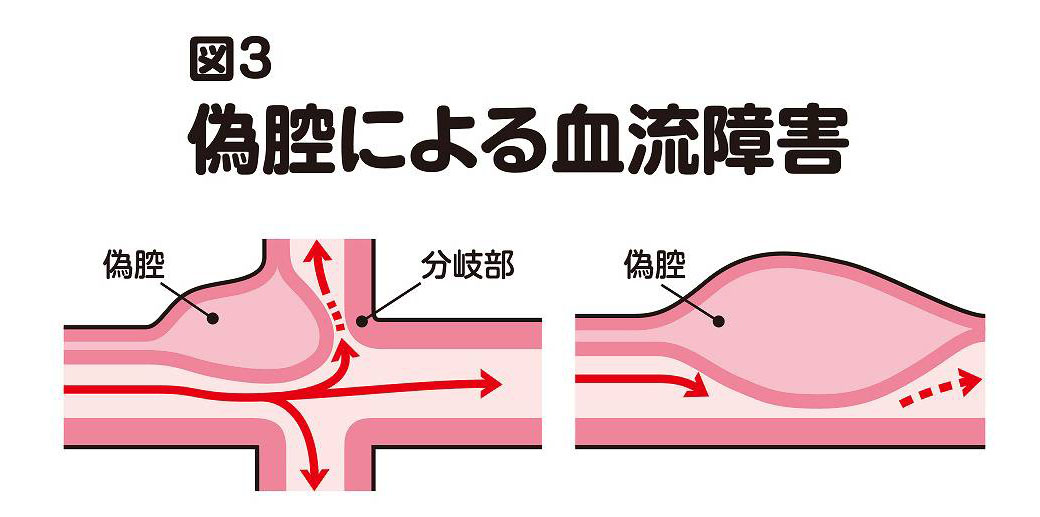
偽腔がもたらす血流障害
偽腔ができることによって、本来の血流が阻害されます(図3)。
大動脈は、いろいろな臓器に血液を送るために、ところどころで枝分かれをしていますが、そうした分岐部に解離が及ぶと、偽腔が枝分かれした血管を塞ぎ、その先の臓器に血が流れにくくなってしまいます。また、大動脈自体も、偽腔が拡大すると本来の通り道である真腔が狭められ、血が流れにくくなってしまいます。
大動脈解離がもたらす危険
大動脈解離のもつ3つの病態が、それぞれ危険な状態を招きます。
【大動脈が膨れる(拡張)】
大動脈が膨れると、大動脈弁閉鎖不全症(心臓から大動脈に血液を送る弁が大動脈の拡張に伴い広がって、心臓の拡張期にきちんと閉じなくなり、血液が心臓に逆流してしまう病気)が起こることがあります。また、声帯を動かす反回神経が拡張したコブに圧迫されることで声がかすれたり(これを「嗄声[させい]」と言います)、嚥下[えんげ]障害(ものが飲み込みにくくなる状態)が起こったりもします。
【大動脈が破れる(破裂)】
大動脈が破れ血管外に出血すると、心タンポナーデ(心臓を包んでいる膜の中に出血したために、心臓が動けなくなる状態)が起こったり、血胸(胸腔内に血が溜まった状態)が起こったりします。大動脈が破裂すると、出血性のショックで急死する可能性が高まります。
【偽腔による圧迫で血が流れなくなる(血流障害)】
偽腔による圧迫で枝分かれした血管が塞がれ、各臓器に血液が届きにくくなると、狭心症、心筋梗塞、脳の虚血(虚血とは血が足らなくなること)、脳梗塞、腸管の虚血、腎不全、上肢の虚血、下肢の虚血、脊髄の虚血(症状としては対麻痺[ついまひ]=両側の下肢の運動麻痺)などが起こります。
大動脈解離が起こってすぐの時期は、強い血流を偽腔の薄い外膜のみで支えているために、きわめて破裂しやすい状態にあります。上行[じょうこう]大動脈(心臓を出てすぐの、心臓に近い大動脈)で解離が起こった場合、無治療で放置すると、1時間に1%ずつ死亡率が上がり、発症して48時間(2日間)以内に約半数の人が亡くなる、と言われています。男女ともに70代に最も多く発症すると言われていますが、40代や50代での発症も稀ではありません。
大動脈解離と解離性大動脈瘤の違い
大動脈解離と解離性大動脈瘤(大動脈瘤解離とも言います)は、言い方が違うだけで、基本的に同じものです。
大動脈瘤というのは、動脈硬化などによって大動脈壁の弱くなっているところがコブ状に膨らんだものですが、この大動脈瘤の中の解離性のもの(血管壁がはがれるもの)を解離性大動脈瘤(大動脈解離)と呼んで、解離のない大動脈瘤と区別しています。治療方法などに多少の違いがあるからです。
大動脈解離の多くはコブ状の膨らみを形成しますが、それほど血管が拡張していないもの(コブの形成が顕著でないもの)でも、治療上は解離性大動脈瘤として扱います。
分類
大動脈解離の分類は、解離が起こった場所、あるいは発生してからの時間経過(病期)によってなされます。
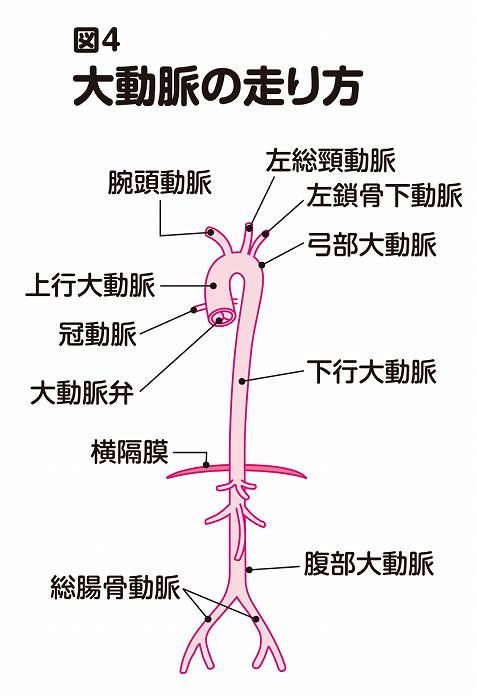
大動脈の走り方
分類の説明に入る前に、前提の知識として、大動脈の走り方を説明します(図4)。
大動脈は、心臓を出てすぐは上方に向かいます。この上に向かう大動脈を「上行大動脈」と言います。直径3センチくらいの太さがあります。ここからは、心筋(心臓の筋肉)に血液を送る冠動脈[かんどうみゃく]が分岐しています。
上行大動脈は、やがて弓状に弧を描いてUターンし、下行[かこう]します。この弓状の部分を「弓部[きゅうぶ]大動脈」と言います(「大動脈弓」とも言います)。ここには上方に3本の大きな分岐(腕頭[わんとう]動脈、左総頸[ひだりそうけい]動脈、左鎖骨下[ひだりさこつか]動脈)があり、それらを通して脳や左右の腕に血液が送られています。
弓部大動脈は、下行しながら心臓の後ろ側(背中側)に回り、下半身へと向かいます。この下行する大動脈のうち、横隔膜から上を「下行大動脈」、横隔膜から下を「腹部大動脈」と言います。また、上行大動脈、弓部大動脈、下行大動脈を総称して「胸部大動脈」と言います。
腹部大動脈からは、肝臓や胃腸、腎臓などの腹部臓器に向かう血管が枝分かれしています。大動脈は下行するにつれ少しずつ径を狭め、腹部大動脈では直径2センチほどの太さになっています。
腹部大動脈は、臍の高さで左右の総腸骨[そうちょうこつ]動脈に分かれます。これらは、骨盤内の臓器や両足に血液を運ぶ役割を担っています。
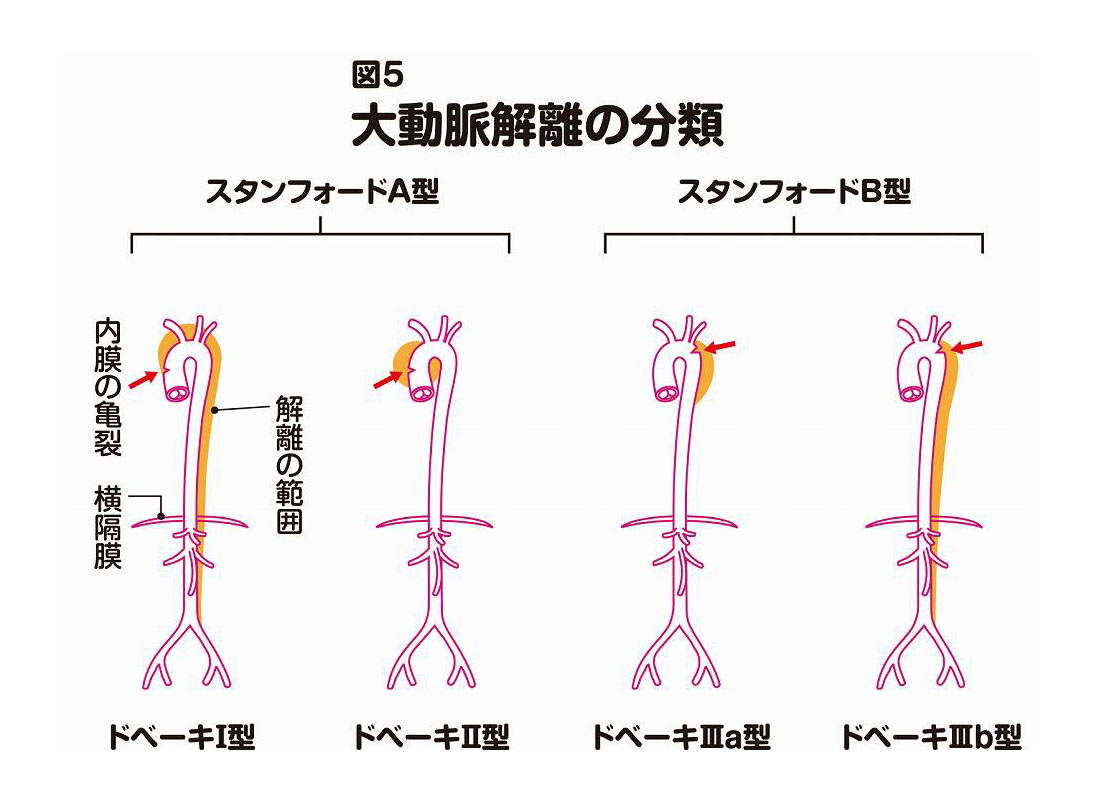
スタンフォード分類とドベーキ分類
解離が起こった場所による分類には、スタンフォード(Stanford)分類とドベーキ(DeBakey)分類があります(図5)。
スタンフォード分類は、予後や治療方針の決定に役立つ分類で、大動脈解離をA型とB型に分けます。A型は上行大動脈に解離があるもの、B型は上行大動脈に解離がないものです。A型のほとんどが緊急手術を要し、一般的に予後も不良です。
ドベーキ分類は、解離の進展範囲とエントリー(血液の偽腔への流入口となる内膜の亀裂)の位置によるもので、Ⅰ型、Ⅱ型、Ⅲa型、Ⅲb型の4つに分かれます。
Ⅰ型は、エントリーが上行大動脈にあり、解離が下行大動脈や腹部大動脈にまで及ぶもの、Ⅱ型は、エントリーやリエントリー(再流入口)が、上行大動脈や弓部大動脈に納まるもの、Ⅲa型は、エントリーが下行大動脈にあり、解離が横隔膜内に及ぶもの、Ⅲb型は、エントリーが下行大動脈にあり、解離が横隔膜より下にまで及ぶものです。
病期による分類
【急性期】
発症後、2週間以内のものです(急性大動脈解離)。
【亜急性期】
発症後、3週間目から2か月以内のものです。
【慢性期】
発症してから2か月以上経ったものです。
大動脈解離の原因
大動脈解離の原因としては、動脈硬化、高血圧、高脂血症、糖尿病、睡眠時無呼吸症候群、喫煙、ストレス、マルファン(Marfan)症候群などの先天的な(生まれつきの)遺伝性疾患、などが考えられます。特に高血圧は重要な危険因子です。
マルファン症候群というのは、遺伝子の異常により組織と組織を繋ぐ結合組織が弱くなって、全身で細胞の弾力性がなくなる病気です。血管壁を弱体化させて解離などを引き起こすだけでなく、心臓の弁を壊したりもします。このほか、遺伝性の危険因子に嚢胞性中膜壊死[のうほうせいちゅうまくえし]などがあります。
大動脈解離が起きる前兆
大動脈解離には前兆といえるものがなく、発症の予測はきわめて困難です。
万一、何の前触れもなく胸や背中に激痛が起こったら、迷わず救急車を呼んでください。
突然、胸や背中に激痛が走る病気で、様子を見ていて大丈夫なものはありません。一刻も早く医療機関を受診してください。
大動脈解離の発症は、夏場に少なく、冬場に多い傾向にあります。また、夜よりも日中に多く、特に午前中(6時から12時くらいの時間帯)に発症することが多いと言われています。
症状・痛み
大動脈解離の症状の一番の特徴は、突然、胸あるいは背中に杭が刺さるような激痛が走ることです。解離が進むにつれ、痛みが胸から腹、脚など、体のいろいろなところに移動する場合があります。
このほか、解離した場所や偽腔が血流をさえぎった場所によって、さまざまな症状が現われます。
【大動脈基部(心臓から出てすぐのところ)で解離が起こる】
基部の拡張につれ大動脈弁も拡張して、血液が逆流する大動脈弁閉鎖不全症となり、呼吸困難や急性心不全(心臓の機能低下)などが起こります。大動脈が破裂して心タンポナーデが起こると、血圧が低下し、ショックに陥ることがあります。
【偽腔が冠動脈を塞ぐ】
狭心症や心筋梗塞が起こり、胸の痛みや圧迫感が生じ、急性心不全を引き起こします。
【偽腔が弓部から出る分枝血管を塞ぐ】
脳への血流がさえぎられ、意識が消失したり、麻痺が起こったりします。また、上肢への血流がさえぎられ、上肢の血圧に左右差が出たり、上肢に冷感が出たりします。
【偽腔が腹腔動脈や上・下腸管膜動脈を塞ぐ】
腸管への血流がさえぎられ、腹痛や腰痛、下血などが起こります。また、肝機能障害が起こります。
【偽腔が前脊髄動脈を塞ぐ】
脊髄への血流がさえぎられ、両側の下肢に運動麻痺(対麻痺)などが出ます。
【偽腔が腎動脈を塞ぐ】
腎臓への血流がさえぎられ、腎梗塞や腎不全を起こします。
検査・診断方法
大動脈解離の検査には、胸部X線検査、心エコー(超音波)検査、造影CT検査、MRI(磁気共鳴画像)検査などがあります。
胸部X線検査
X線を当てて胸部を調べる検査です。
大動脈解離が起こっていると、大動脈陰影の急速な拡大が見られます。また、上縦隔[じょうじゅうかく]の拡大が見られることもあります(縦隔とは、胸腔の中の左右の肺に挟まれた領域で、心臓はこの縦隔の中にあります)。
心エコー(超音波)検査
人間の耳に聞こえない高い周波数の音波(エコー)で体の中を探る検査です。体の外から簡便に内部が探れるため、ベッドサイドで緊急に実施できるという利点があります。
解離が起こっていると、上行大動脈内に波状に動くフラップ(偽腔と真腔を隔てる血管壁)が認められる場合があります。大動脈弁閉鎖不全症、心筋梗塞、心タンポナーデなどの合併症の有無や程度を調べるのに有用です。
造影CT検査
造影剤を体内に入れX線で断層撮影する検査です。胸部X線検査や心エコー検査で大動脈解離が疑われた場合、この造影CT検査で最終診断を下します。
これで得られた画像には、真腔や偽腔、フラップなどが映し出されます。また、スタンフォードA型かB型か、枝分かれした動脈が閉塞しているかどうか、解離が大動脈基部に及んでいるかどうかなど、診断と治療に必要な情報が得られます。
MRI(磁気共鳴画像)検査
磁気の力を使って臓器や血管を撮影する検査です。さまざまな断面で鮮明な画像が得られます。解離の範囲や状態が把握できます。
治療方法
大動脈解離の治療は、スタンフォードA型とB型で違ってきます。
上行大動脈に解離があるA型は、急死に至る合併症(心タンポナーデ、心筋梗塞、大動脈弁閉鎖不全症、急性心不全など)を生じやすいため、緊急手術が必要です。
一方、上行大動脈に解離がないB型は、大動脈が破裂していたり、血液が充分に届かず臓器に障害が起こったりしているときには緊急手術が必要ですが、それ以外は、まずは血圧を下げ、解離がそれ以上進行しないよう、また、合併症が起こらないよう管理します。
スタンフォードA型の治療
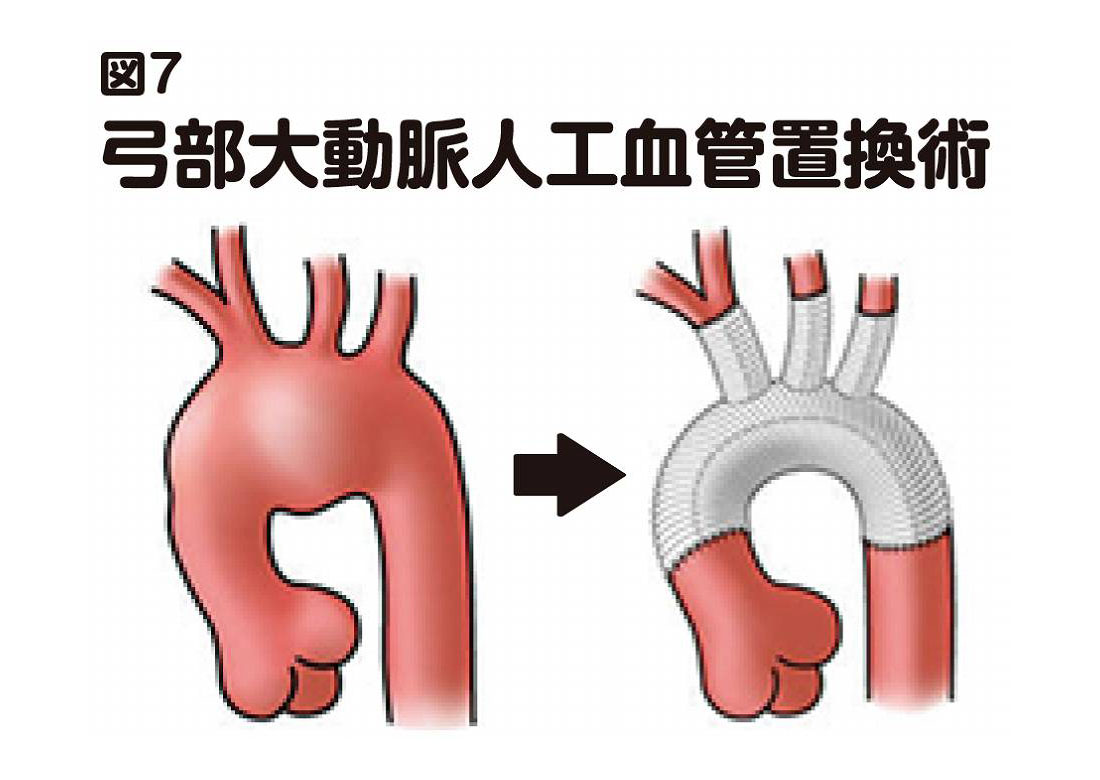
A型の解離に対する手術としては、上行大動脈への人工血管置換術、あるいは上行大動脈プラス弓部大動脈への人工血管置換術などが行なわれます。解離し損傷した血管を人工血管(図6)に置き換える手術です。
スタンフォードB型の治療
大動脈が破裂していたり、各臓器に充分な血液が届かなくなっていたりする場合は、B型の解離であっても、下行大動脈や腹部大動脈への人工血管置換術、あるいはステントグラフト内挿術やハイブリッド治療が行なわれます。
解離の範囲が局限され、各臓器への血流が維持されている場合は、薬物治療(血圧を下げる降圧治療)を行ないながら、経過を観察します。
降圧治療は、収縮期の血圧(上の血圧)を100~120mmHg以下に維持することを目標とします。まず使われるのは、交感神経(心臓の働きを活発にする神経)の働きを抑えるベータ遮断薬で、それだけでは充分に血圧が下がらない場合は、他の降圧剤を併用します。
手術方法3つ
大動脈解離の手術方式には、人工血管置換術、ステントグラフト内挿術、ハイブリッド治療の3つがあります。
①人工血管置換術
人工血管置換術は、主に上行大動脈や弓部大動脈の解離に対して行なわれます(図7)。
手術では、まず胸を切り開き、心臓の動きを止め(高濃度のカリウムを含む心筋保護液を入れると、心臓が一時的に動きを止めます)、人工心肺に繋いで全身への血流を確保します。そのうえで、解離した血管を取り除き、人工血管を縫い付けます。
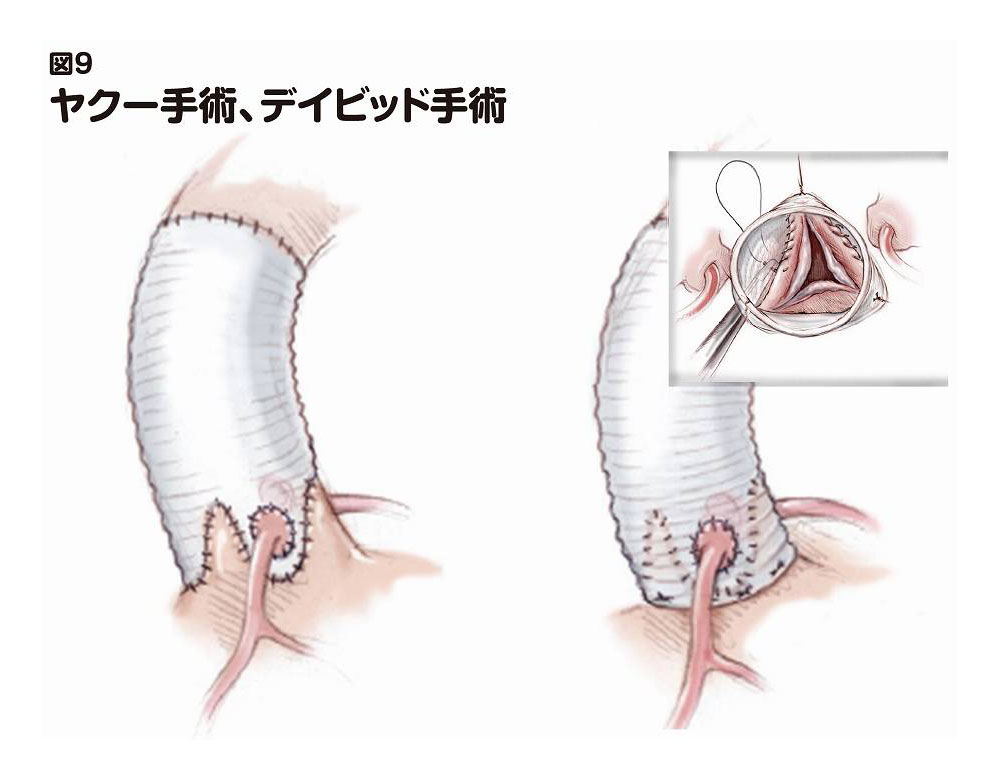
大動脈基部(心臓を出てすぐの大動脈)に解離が及び、それにつれ大動脈弁の弁輪(弁の外周)が拡大している場合(大動脈弁閉鎖不全症)、弁付きの人工血管を用いて、弁も一緒に取り換えることがあります(これをベントール〔Bentall〕手術と言います。図8)。弁の状態が良好な場合は、弁を温存するヤクー(Yacoub)手術やデイビッド(David)手術(図9)を行ないます。
弓部大動脈を人工血管に取り換える手術では、脳や上肢に枝分かれしている血管も再建しなければなりません。手術しているさなかに、脳に血液が行かなくなったりすると大変なので、高度で慎重な手術が求められます。
軽度低体温手術
心臓を止め、人工心肺で血流を確保する場合、一番問題になるのが、最も虚血に弱い脳の保護です。脳は、摂氏37度において5分間血が行かなくなると、不可逆的な(元に戻らない)脳障害が起こるとされています。それで、これまでは手術に際し、摂氏20度前後の超低体温にすることで脳の代謝を低下させ、虚血許容時間を延長させてきました。
しかし、この方法では脳梗塞や感染症、肺炎などのリスクが高まり、出血も止まらず、手術も1日がかりとなります。死亡率も高い状態です。
そこで、ニューハート・ワタナベ国際病院では、超低体温ではなく、摂氏32度の軽度低体温で手術を行なっています。これまでにこの手術による死亡例はなく、合併症も減っています。
また、縫合でも出血しない方法を採用したことで、4時間程度で手術を終えることができます。輸血なしに手術ができるため、大量輸血が引き起こす副作用も防げます。
ただし、この軽度低体温手術には、医師に手早い完璧な技術が求められます。
②ステントグラフト内挿術
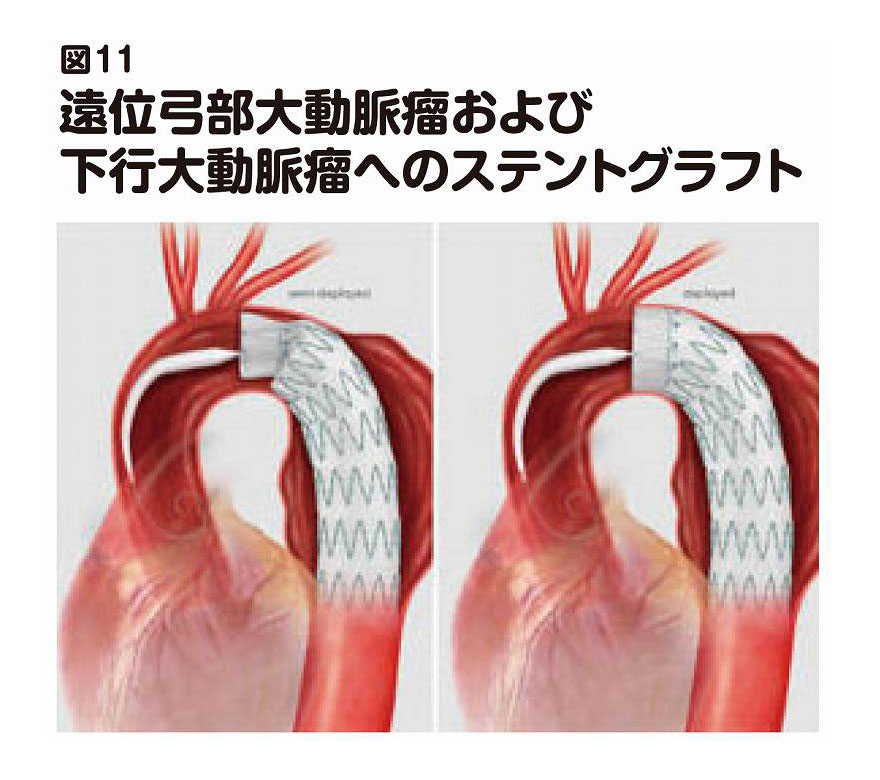
ステントグラフトとは、人工血管にステントと言われるバネ状の金属を取り付けたものです(図10)。これを圧縮した状態でカテーテル(細い管)の中に収納し、カテーテルを治療する部位(解離したところ)にまで運び(足の付け根などから動脈に入れて移動させます)、その場所でステントグラフトを広げて留置します(図11)。
人工血管置換術が「傷んだ水道管を取り換える」ようなものだとしたら、こちらは「傷んだ水道管を内側から補強する」ようなものだと言えるでしょう。
比較的新しく、1990年代初頭から欧米を中心に臨床応用されてきた技術で、高齢の患者さんなど、体力のない人に対して行なわれてきましたが、現在、下行大動脈や腹部大動脈の解離においては、このステントグラフト内挿術を行なう病院が増えてきています。解離の範囲によっては、2つないし3つのステントグラフトを繋げてゆくこともあります。
ステントグラフト内挿術のメリット、デメリット
メリットは、人工血管置換術が胸を切り開く手術であるのに対し、こちらはカテーテルを利用した傷の小さな手術である、という点です。そのため、手術後の痛みが少なく、手術時間も入院期間も短くなります。出血量が少ないので輸血を必要とすることも稀です。血管の損傷、臓器虚血、血栓塞栓症などといった合併症の発生率は、人工血管置換術よりも低いレベルにあります。
人工血管置換術に比べると、人工心肺を使わずに済み、心臓を止める時間も短くできて、患者さんにとって体の負担が少ない手術になります。
デメリットは、手術中や手術後、発熱や胸水貯留などが比較的高率に発生することです。また、退院後も、ステントグラフトの変形・破損・移動・感染などに注意が必要です。
③ハイブリッド治療
大動脈から主要な血管が枝分かれしている箇所に解離が及んでいると、ステントグラフトは使えません。そこにステントグラフトを留置すると、枝分かれした血管を塞いでしまうからです。そこで、そんな場合には、人工血管によるバイパス手術(血流の迂回路を作る手術)とステントグラフトを組み合わせた治療を行なうことがあります(図12)。これをハイブリッド治療と言います。
弓部大動脈と下行大動脈にコブがあるもの(左)を、まず弓部を人工血管に置き換え、枝分かれている左総頚動脈とつなぐ(中)。ステントグラフトを装着したカテーテルを下行大動脈に入れ(中)、ステントグラフトを広げる(右)。ステントグラフトで左鎖骨下動脈がふさがれるが、バイパスがあるので血流は確保できる。
ハイブリッド治療を行なえば、ステントグラフトの留置で塞がれた血管にも、バイパスを通して血液が流れます。
予後
大動脈解離の予後には、患者さんに慎重な姿勢が求められます。
破裂や臓器不全を起こす危険性の高い血管を手術で人工血管に置き換えたとしても、それ以外の血管のかなりの部分は、解離したままの状態で残っています。また、解離を起こしやすい体質もそのままなら、解離を呼ぶ生活習慣もすぐには変えられるものではありません。
したがって、この先、解離が拡大し破裂しないよう、日々の血圧の管理などが求められます。また、病院での定期的な経過観察も必須です。急性期を乗り切った、と安心し、楽観するのは禁物なのです。
なお、残存している解離が拡張傾向にあると分かったら、再発症する前に治療を受けることをぜひお勧めします。まだ何の症状も出ていないときに手術を受ける決断をするのは、なかなか大変ではありますが、発症してから緊急に行なう手術も、発症する前に充分な準備をして臨む手術も、行なうことは同じです。であれば、より安全性の高い発症前に実施すべきでしょう。
大動脈解離について少しでも不安をお持ちの方は、まずはオンライン診療をご利用下さい。
予防方法・対策
大動脈解離の予防方法は、まずは、危険因子と思われる動脈硬化、高血圧、糖尿病、高脂血症などの生活習慣病にかからないようにし、すでにかかっている人は、それらの改善を心がけることです。特に高血圧は大敵です。食事は塩分を控えめにしましょう。また、ストレスを溜めないようにし、タバコもやめましょう。
まとめ
大動脈解離は、何の前触れもなく胸や背中に激痛が走る病気で、放置すると死に至ります。躊躇することなく救急車を呼びましょう。また、手術で急性期を乗り切っても、解離は進行しがちです。退院後の経過観察は欠かせません。
生活習慣病、とりわけ高血圧には気をつけ、タバコはやめましょう。